器官對體液與電解質的調節
重點整理
- 全身體液主要由腎臟系統調節。
- 腎臟會反覆循環約 5 至 6 公升血液,且在選擇性再吸收前每日可產生約 200 公升濾液。
- 當體液不足(低血容量)時,抗利尿激素(ADH)釋放增加,促進腎臟水分再吸收。
- 當腎小管液體容積高時,ADH 受抑制,導致尿液更稀釋。
- 血清滲透壓正常約為 275-295 mmol/kg,反映血液濃縮狀態。
- Osmolality 是每公斤溶劑中的溶質粒子數,而 osmolarity 是每公升溶劑中的溶質粒子數。
- 尿比重正常約 1.010-1.020;數值偏高提示濃縮,偏低提示稀釋。
- 口渴、下視丘滲透壓受器、ADH 與 RAAS 共同協調血管內容積與血壓。
- RAAS 可由低血壓或低血清鈉啟動,增加血管張力與鈉水滯留,同時促進鉀排泄。
- 醛固酮是腎生理中調節鈉與鉀處理的關鍵,並透過鈉再吸收支持水分滯留。
- 在穩定成人中,每日體液排出以腎臟為主(約 60%),其餘為皮膚/GI/肺不顯性流失(約 40%)。
- 心臟利鈉肽在體液過負荷時會透過促進血管擴張與鈉水排泄來拮抗 RAAS。
- 恆定控制透過受器 → 控制中心 → 效應器訊號迴路來矯正偏離設定點。
- 負回饋是主要恆定迴路型態,會藉由逆轉偏離來使狀態回歸正常範圍。
- 正回饋會放大刺激以快速完成特定生物事件,且必須及時終止以避免不穩定。
- 高滲透壓與低滲透壓若未及時矯正,皆可造成嚴重神經惡化。
- 感知、迴路啟動、反應執行或設定點調節任一環節失效,都可能進展為細胞損傷與器官功能障礙。
- 電解質異常常彼此依賴,因此單一重度失衡可引發多電解質連鎖反應。
病理生理
體液與電解質恆定仰賴器官系統與荷爾蒙的交互作用,而非孤立檢驗值。腎臟調節全身體液,並透過 ADH 調節來回應腎小管壓力與容積狀態。腎絲球過濾依賴壓力:腎絲球微血管靜水力支持濾液形成,而腎灌流壓下降會降低廢物與液體清除。
當體液流失且血管內鈉濃度上升時,血清滲透壓增加。下視丘滲透壓受器會觸發口渴並增加 ADH 釋放,進而促進腎臟保水。此調節路徑仰賴可獲得液體,且病人需能在出現口渴時飲水。
RAAS 也會在低壓與低鈉狀態下支持灌流。血壓下降或血清鈉下降會刺激腎臟釋放 renin。Renin 將肝臟來源 angiotensinogen 轉為 angiotensin I,而肺部 angiotensin-converting enzyme 將 angiotensin I 轉為 angiotensin II。Angiotensin II 造成血管收縮並刺激 aldosterone 釋放,增加腎臟鈉再吸收,使水分回到血管內,同時增加鉀排泄。
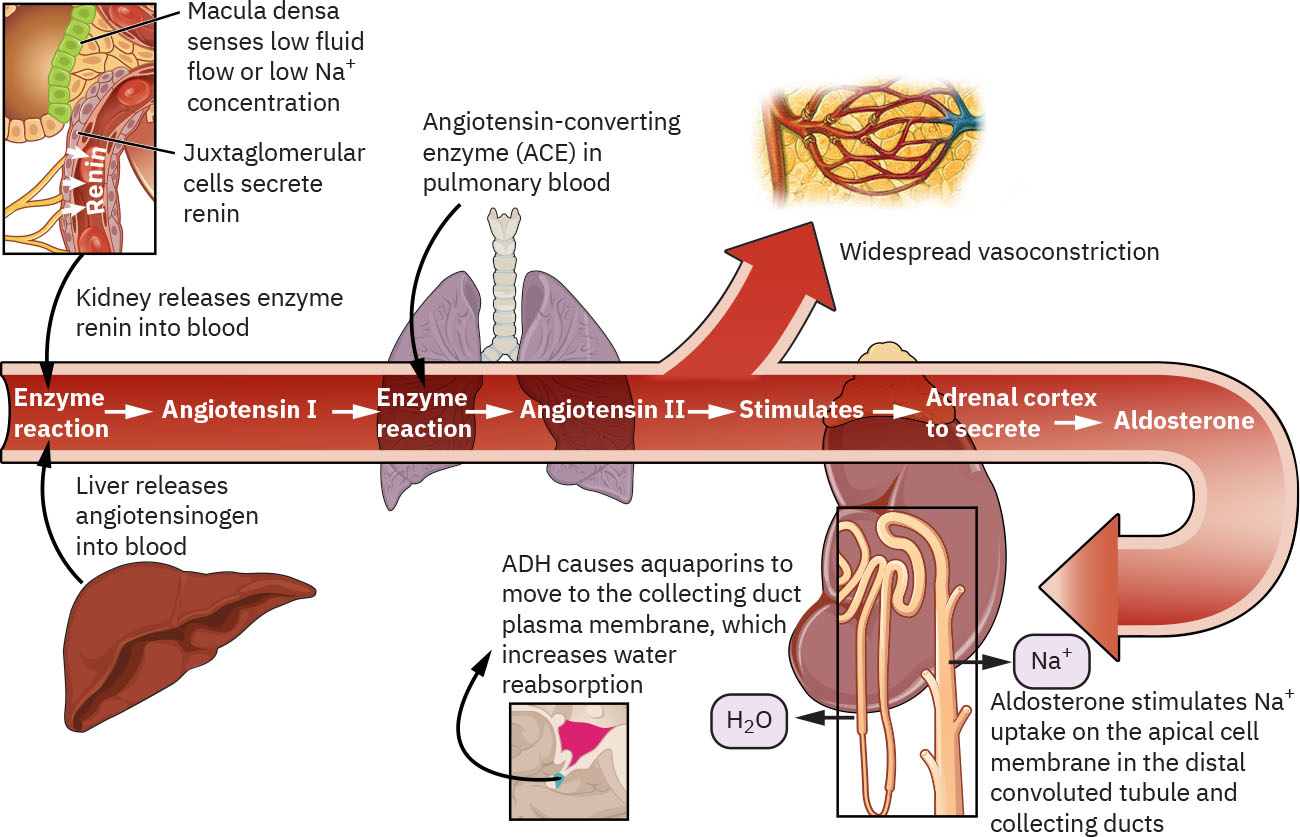 Illustration reference: OpenStax Clinical Nursing Skills Ch.19.1.
Illustration reference: OpenStax Clinical Nursing Skills Ch.19.1.
利鈉肽在生理上與 RAAS 對抗。當心臟組織感知體液過負荷與壓力上升時,這些胜肽會促進血管擴張與腎臟排鈉,以降低循環容積與壓力。 除 ADH、RAAS 與利鈉肽外,胰島素、腎上腺素、糖皮質素與副甲狀腺軸荷爾蒙等內分泌因素,也會影響特定電解質型態。 Renin 釋放部分受腎絲球旁器調節,該結構鄰近腎絲球,將腎元灌流感測與 RAAS 啟動直接連結。
在攝取充足情況下,腎臟通常每日產生約 1,500 mL 尿液。少尿是體液不足與腎損傷路徑中的早期警訊,應結合脈絡做趨勢追蹤。
分類
- Volume-conserving response: 低血容量時 ADH 增加,水分再吸收上升。
- Volume-excreting response: 腎小管液體容積高時 ADH 抑制,導致稀釋尿。
- Osmoreceptor-thirst response: 血清滲透壓升高會驅動口渴與 ADH 釋放。
- Osmolality measurement domain: Osmolality 量化每 kg 溶劑粒子;osmolarity 量化每 L 溶劑粒子。
- Hyperosmolality pattern: 高溶質狀態(例如脫水或糖尿病相關狀態),有循環壓力與神經症狀風險。
- Hypoosmolality pattern: 低溶質狀態(例如過多游離水或水平衡失調),有腦水腫與神經惡化風險。
- RAAS pressure-restoring response: Renin → angiotensin II → aldosterone 會增加血管張力與鈉水滯留。
- RAAS sequence detail: Renin + angiotensinogen(liver)→ angiotensin I → ACE(lungs)→ angiotensin II。
- Natriuretic-peptide counterregulation: 心臟胜肽在體液過負荷/高壓時會促進血管擴張與鈉水排泄。
- Feedback-loop control architecture: 受器偵測、中央整合與效應器反應共同矯正體液/電解質偏移。
- Negative-feedback loop pattern: 抑制性反應會降低初始偏離,使變項回到設定點。
- Positive-feedback loop pattern: 放大反應會增加初始刺激直到終點完成(例如凝血、泌乳排出反射與分娩子宮收縮)。
- Homeostatic-failure modes: 偵測失效、回饋啟動失效、效應器反應失效、設定點失調。
- Sodium regulation pathway: 腎臟系統,受 aldosterone 影響。
- Potassium regulation pathway: 腎臟系統,受 aldosterone 並加上 insulin、epinephrine 與 glucocorticoids 影響。
- Calcium regulation pathway: 骨骼-內分泌交互作用,涉及 parathyroid hormone、vitamin D 與 calcitonin。
護理評估
NCLEX 重點
先將症狀對應到最可能的受調節電解質路徑,再用檢驗與容量趨勢驗證。
- 追蹤 intake-and-output、尿液濃縮型態與淨體液平衡,以評估 ADH 相關容積線索。
- 當稀釋或濃縮狀態不明時,趨勢比較血清滲透壓與尿液滲透壓/比重型態。
- 評估功能障礙(認知改變、虛弱、液體可近性差)是否限制對口渴線索的反應。
- 評估低灌流代償型態(例如低血壓伴心搏過速),此現象可先於腎過濾惡化。
- 對 鈉失衡,評估意識混亂、易怒、口渴、黏膜乾燥、頭痛、癲癇風險與昏迷進展。
- 對 鉀失衡,評估 GI 絞痛、無力、脈搏品質,以及 ECG 的高尖或低平/倒置 T 波與 U 波型態。
- 對 鈣失衡,評估 GI 症狀、肌無力、刺麻、抽筋與手足搐搦。
- 對低尿量趨勢升級處置,包括持續 8 小時尿量低於 30 mL/hour(或低於 0.5 mL/kg/hour)。
- 將症狀型態與連續生化數值及臨床軌跡相互對照。
- 當體液滯留惡化但尿量下降時,考慮混合型態:血清更稀釋而尿液仍相對濃縮。
護理措施
- 當容積或神經趨勢提示代償調節失效時,優先及早介入。
- 協調連續檢驗與聚焦再評估,以判定器官層級調節是否正在恢復平衡。
- 執行醫囑輸液策略,並監測尿液反應是否符合預期 ADH 相關效應。
- 將每日出入量型態與成人預期水平衡範圍比對(穩定狀態約攝取 2,500 mL、排出 2,500 mL)。
- 對慢性腎臟與內分泌風險病人強化鈉與鉀管理衛教。
- 當 ECG 或神經發現顯示嚴重電解質不穩定時,快速升級處置。
代償極限
器官-荷爾蒙代償在急性狀態具保護作用,但在慢性疾病或重度失衡中無法完全阻止惡化。
藥理學
| Drug Class | Examples | Key Nursing Considerations |
|---|---|---|
| diuretics | Loop and potassium-sparing categories | 利尿劑會改變鈉、鉀與體液平衡,需密切趨勢監測。 |
| intravenous-fluid-categories-tonicity-and-infusion-regulation (electrolyte-replacement-therapy) | Sodium or potassium replacement protocols | 矯正需由連續檢驗、腎臟狀態與症狀嚴重度共同引導。 |
臨床判斷應用
臨床情境
一位 慢性腎臟病 病人出現體液滯留、電解質異常與逐漸惡化的神經症狀。
- 辨識線索: 體液平衡異常、尿液型態改變,以及令人警訊的鈉/鉀症狀輪廓。
- 分析線索: 腎臟-內分泌調節未能維持恆定。
- 優先假設: 立即風險包括神經惡化與心臟傳導不穩定。
- 提出解決方案: 強化監測、取得連續檢驗/ECG,並執行醫囑容積-電解質矯正。
- 採取行動: 升級惡化並執行病因導向管理。
- 評估結果: 尿量、檢驗與症狀趨向穩定基線。
相關概念
- 鈉平衡失調 - 鈉表現可對應至腎-醛固酮調節失效或過負荷型態。
- 鉀平衡失調 - 鉀不穩定反映腎處理與荷爾蒙調節轉移。
- 體液容積不足、低血容量與脫水 - 低容積狀態會驅動 ADH 介導保水。
- 體液容積過多(高血容量) - 高容積狀態可伴隨 ADH 抑制與稀釋型態。
- 腎臟疾病 - 慢性腎功能失調會降低維持體液-電解質恆定能力。
自我檢核
- 在低血容量與高腎小管液體容積狀態下,ADH 行為有何不同?
- 哪些症狀群可提示鈉、鉀與鈣失調?
- 為什麼慢性腎臟病病人即使荷爾蒙路徑已啟動,代償仍可能失敗?