多模式疼痛管理与 PCA 安全
关键要点
- 多模式疼痛管理将药物与非药物干预结合,可获得更好结局。
- 阿片类治疗需严密监测镇静、呼吸抑制、依赖与过量风险。
- 非阿片类与辅助治疗可在降低阿片负担同时扩展控制能力。
- 在正确患者筛选、泵程序设定、双人核验与再评估流程到位时,PCA 才安全有效。
病理生理学
疼痛由生物、心理与社会因素共同介导;单一模式治疗常残留痛苦负担。多模式策略可同时靶向多个机制,在提高缓解效果同时限制任一药物类别因加量带来的毒性。
阿片类可降低疼痛信号,但也会抑制呼吸驱动与认知。非甾体抗炎药(NSAIDs) 与对乙酰氨基酚(acetaminophen)靶向炎症与伤害感受通路,而辅助药物可支持神经病理性、痉挛性或局部疼痛状态。
非药物干预(运动治疗、引导意象、按摩、环境调节、认知策略)可减少中枢放大并改善功能、应对与生活质量。
若术后疼痛控制不佳,应激激素信号(如皮质醇过高)、高血糖倾向、炎症持续与活动减少会减慢组织愈合与康复进度,同时增加并发症风险。
分类
- 药物核心:阿片类、非阿片类与辅助镇痛分层。
- 非药物核心:躯体、心理、情绪与环境干预。
- 严重度阶梯情境:轻/中/重度疼痛类别可指导分步药物升级。
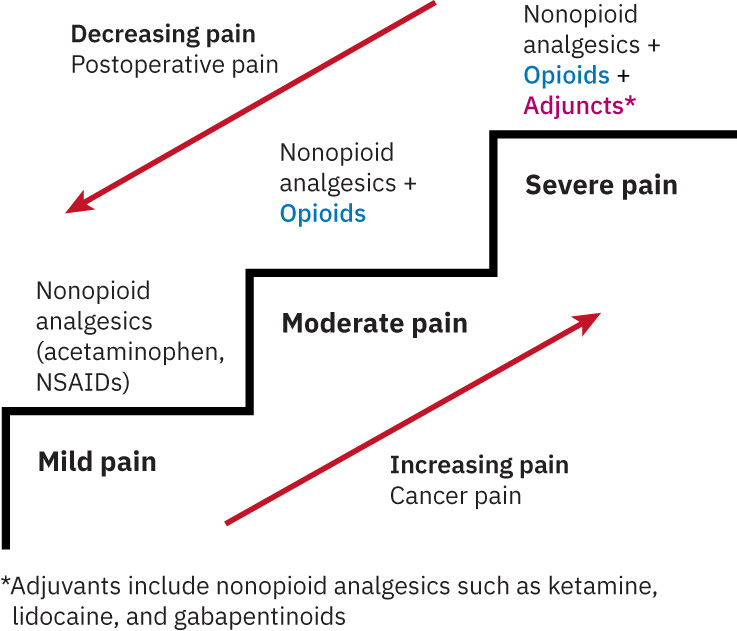 Illustration reference: OpenStax Medical-Surgical Nursing Ch.7.3.
Illustration reference: OpenStax Medical-Surgical Nursing Ch.7.3.
- PCA 结构:负荷剂量、按需(推注)剂量、基础输注率(如使用)、锁定间隔与 1 小时最大限量。
- 安全领域:候选者筛选、监测、不良反应预防与文书完整性。
- 照护标准领域:入院/急诊疼痛筛查、年龄/病情适配再评估、功能目标追踪与阿片风险出院教育。
护理评估
NCLEX 重点
疗效评估应看“功能与安全趋势”,而不只看镇痛强度。
- 评估疼痛机制与严重度模式,以选择药物类别组合。
- 在住院场景中,确保入院(及适用时急诊入科)进行疼痛筛查,并用与年龄、认知和沟通能力匹配的工具再评估。
- 对新发重度疼痛或当前方案无反应疼痛及时升级;突发重痛或胸痛/压榨痛需按流程立即急症响应。
- 将“慢性疼痛治疗中仍持续重度突破痛”视为更高急性度升级线索,可能需要高级住院管理。
- 描述突破痛触发模式(如活动、应激/疾病波动、剂末失效或无诱发发作),以决定仅救援治疗是否足够,或需修订基础方案。
- 评估阿片风险因素:镇静易感性、呼吸受损风险、合并镇静药使用。
- 选择前评估非阿片风险谱(如老年、妊娠、肝/心血管/肾/胃肠道(GI)合并症情境)。
- 评估 PCA 适配性:认知状态、遵循指令能力与禁忌证谱。
- 按机构政策明确评估 PCA 禁忌证谱(如阿片过敏、活动性感染担忧、颅内压升高、重度肾功能障碍或出血风险情境)。
- 将意识混乱或过度镇静视为 PCA 排除线索,因为安全 PCA 依赖清醒且自主按键。
- 评估阿片误解(如担心短期术后使用即成瘾)导致的镇痛依从下降。
- 在术后路径中,强化“急性术后短期阿片使用”与“物质使用障碍”不同,同时继续执行标准安全监测。
- 对已知 SUD 病史患者,预判耐受导致术后阿片需求可能更高,并协作升级个体化给药。
- 对成人初级照护阿片使用,评估计划是否与美国疾病控制与预防中心(CDC)处方领域对齐:启动必要性、阿片选择/剂量、初始疗程与随访、风险伤害缓解。
- 在门诊阿片开具或续方前,核验处方药监测计划(PDMP)管制药史;若持续慢性阿片治疗,按政策/指南至少每 3 个月复核 PDMP。
- 评估非药物治疗反应与患者依从障碍。
- 评估所选非药物方式为“补充治疗”(与药物联合)还是“替代治疗”(替代药物),并核验各路径安全性/目标匹配。
- 评估当前全部天然产品使用(草药、维生素、补充剂、精油)与潜在相互作用风险;提醒患者许多补充剂并未像处方药那样由美国食品药品监督管理局(FDA)以同等标准监管安全/有效性。
- 评估电刺激方式(如经皮神经电刺激,TENS)适用性:筛查植入装置状态及主要禁忌情境(如妊娠特异限制、活动性出血、癫痫、癌症或 DVT 风险)。
- 评估无言语、认知受损、文化性压抑疼痛表达及语言障碍人群的低治疗风险。
- 评估患者对疼痛意义、可接受治疗与传统疗法的信念,以预防文化驱动的漏报或拒治。
- 评估恐惧放大模式(如疼痛恐惧、灾难化或回避行为),其可增加主观疼痛并降低功能。
- 当疼痛与既往损伤或虐待相关时,评估创伤与创伤后应激障碍(PTSD)背景,因为未处理创伤可维持疼痛痛苦循环。
- 评估不良应对(如酒精/物质自我用药、严重活动退缩)与保护性习惯(运动、睡眠规律、压力调节)。
- 评估习得性疼痛行为(如因短期缓解而长期不动)是否加重长期疼痛与功能恶化。
- 在重症或临终照护中,评估“保持清醒/意识”是否为优先项,因为这会影响对镇静性镇痛药的接受度。
- 评估实际可及障碍(如口译可用性、药物费用/覆盖与随访可及性)是否降低疼痛计划效果。
护理干预
- 落实用药安全步骤:正确患者/药物/剂量/途径/时间 + 给药后监测。
- 立即在给药记录(MAR/eMAR)中记录已给镇痛药,并及时更新非药物干预记录,以减少重复给药与交接差错风险。
- 对计划康复治疗,协调跨学科预给药时点(常 PT/OT 前 30-60 分钟)以提升参与与安全。
- 在镇痛前后完成疼痛再评估,以确认适应证与反应。
- 若存在恶心/呕吐,与处方者协调选择最有效给药途径;口服吸收/耐受不可靠时避免口服给药。
- 阿片配药/给药时尽量减少干扰,并按政策执行高警示药物独立双人核查流程。
- 发生阿片废弃时,按管制药废弃政策执行并完成见证文书。
- 可行时将药物治疗与至少一种非药物方式配对。
- 对急性软组织损伤,先行 RICE 模式(休息 Rest、冰敷 Ice、加压 Compression、抬高 Elevation),并在首 24-48 小时后随目标从控炎转向愈合与活动恢复而复评进展。
- 有目的地应用热疗/冷疗:僵硬或慢性不适常热敷约 5-20 分钟,急性炎症冷敷最长约 20 分钟;皮肤与冷热源间应有隔离层并常规检查皮肤损伤。
- 避免刻板假设(如“某文化坚忍就不痛”);将自述、行为与临床发现结合制定个体化计划。
- 选择与患者偏好和目标一致的非药物方式(如分散注意、放松、体位、皮肤刺激或身心方法),并按舒适目标记录效果。
- 在住院场景中,对热/冷疗、按摩、针灸/按压与经皮神经电刺激(TENS)等非药物方式先确认是否需医嘱。
- 将非药物试验视为迭代个体化过程:若某方式安全但无效,应更换方法而非完全放弃非药物照护。
- 对慢性疼痛且存在恐惧回避者,结合 CBT/正念应对策略及分级暴露/分级活动方法。
- 使用实用运动方案(物理治疗、低强度锻炼或瑜伽式动作/呼吸)改善活动能力、压力调节与功能。
- 适当时提供特定天然与身心辅助手段(如芳香疗法、引导意象、冥想、正念、CBT 或瑜伽/太极式动作),并记录患者特异获益与负担。
- 可用时采用支持性创意/动物辅助分散方式(如艺术、音乐或宠物疗法路径),以改善放松并降低疼痛信号显著性。
- 对伴炎症模式的慢性疼痛(如纤维肌痛场景),在符合营养目标时强化饮食指导:增加蔬菜、全谷与瘦蛋白,减少精制糖与过量红肉。
- 以文化敏感、语言适配方式进行用药教育,必要时结合图示/示范以匹配健康素养。
- 强化“疼痛管理是患者权利”,且早期治疗比等待重度升级更安全。
- 在合并 SUD 与疼痛时,以“双轨目标”制定计划:充分止痛 + 用结构化防护应对 SUD 风险。
- 指导患者:回避疼痛表达和不报告会延误严重病因诊断/治疗;强化早报告与及时再评估。
- 与患者/家庭共同建立包含功能目标(如呼吸、翻身、行走)而非仅评分目标的现实可测疼痛计划。
- 使用小而可达的功能目标对抗无望感,并随时间强化治疗有效性信号。
- 按严重度与给药途径采用分步方法匹配镇痛强度(适当时先非阿片再升级),优先最低有效剂量与最少侵入途径。
- 在急性重痛轨迹中,教学预期转衔步骤(如 IV 阿片、口服阿片,随后随病情改善转非阿片),使患者可预期“降阶”变化。
- 在术后出院规划中,随恢复稳定将镇痛由 IV 转口服;避免出院前临时追加末次 IV 阿片,因为仍需呼吸监测。
- 灵活应用世界卫生组织(WHO)阶梯逻辑:重度急痛可先从高效力阶梯起步后再降阶;慢性痛常从低阶梯逐步升级。
- 在慢性非癌痛中,若存在有效替代方案应避免常规“阿片优先”;仅在风险-获益评估与监测计划后使用阿片。
- 对阿片使用障碍(OUD)相关疼痛,先最大化非药物与非阿片选项(如运动/物理治疗/CBT、非甾体抗炎药(NSAIDs)、局部药及部分辅助药如 SNRIs/TCAs);若临床确需阿片,不应仅因 OUD 病史而拒绝。
- 在 18 岁以下患者中,若有有效替代方案应避免阿片优先;若确需阿片,使用最低有效剂量并加强监测。
- 对 PRN 镇痛药,加药前核验过去 24 小时已给剂量与累计上限。
- 对门诊 PRN 范围处方(如 1-2 片),指导“先低剂量再复评”,避免不必要过度镇静或过量。
- 对 SUD 风险患者需阿片治疗时,共同建立共享目标/已知风险,使用治疗协议,低起始缓慢滴定并安排密切随访复评。
- 对 PCA,按政策双护士签核核验推注/基础/锁定设置。
- 在儿科,仅当儿童发育/认知可胜任(常 >6 岁且理解充分)时使用 PCA,并强化“仅患者本人按键”。
- 教育患者/家属:除非明确流程另有规定,否则仅患者本人可启动 PCA。
- 对高风险档案(如睡眠呼吸暂停、肥胖、肝肾受损或近期镇静/麻醉暴露)加强 PCA 监测。
- 当阿片治疗进行中保持纳洛酮可即刻获取,并将过度镇静视为即将发生呼吸抑制的早期预警。
- 对阿片初治、近期阿片加量或合并苯二氮卓/镇静药暴露者,加强镇静/呼吸核查。
- 监测常见阿片/PCA 不良反应(如便秘、恶心呕吐、瘙痒、尿潴留)并早期处理以维持依从。
- 及早预判阿片不良反应处理医嘱(如软便剂/泻药与止吐药)以减少治疗中断。
- 按途径与起效时间复评镇痛效果(常 IV 后约 15-30 分钟、口服后约 60 分钟内,按政策);若疼痛仍高于可接受水平,升级药物与非药物方案并通知医师。
- 若突破痛在救援给药后反复发生,应升级修订计划(如调整基础方案 + 触发因素定向非药物支持),而非反复仅做救援循环。
- 对椎管内/植入式阿片给药(如硬膜外或鞘内泵),严密监测剂量/装置并发症;出现戒断体征、神经改变或心肺恶化时立即升级。
- 交接时,进行双护士文书核对“按压次数与实际给药次数”及剩余管制药液量。
- 当存在阿片诱导便秘风险时,监测肠功能并启动预防(液体、早期活动、软便剂/泻药计划)。
- 对复杂疼痛或阿片风险病例,按政策升级转诊路径(如疼痛专科或阿片治疗支持)。
- 对创伤相关疼痛负担,在镇痛照护同时协调创伤知情心理健康转诊路径。
- 在无禁忌时主动启动阿片肠道预防策略(补液、适当纤维/饮食、软便剂/泻药计划、活动)。
- 结合放松、呼吸、CBT 与运动方式,应用环境性非药物支持(光线/噪音/温度优化)。
- 可行时聚合照护任务,减少睡眠中断并在疼痛恢复期保留修复性休息。
- 在操作与日常波动时使用分散策略(音乐、谈话、游戏、引导活动);儿科患者常对年龄适配分散反应良好。
- 在治疗性触碰前筛查禁忌(如活动性皮疹/感染、部分心血管高风险状态、妊娠特异注意),并个体化压力/强度。
- 仅在风险筛查可接受时使用按摩/手法;对抗凝患者及骨折、血栓风险、开放伤口/感染或骨质脆弱情境应避免或升级复核。
- 对针灸路径,转介前确认由受训专业人员执行并完成禁忌筛查(如起搏器情境、抗凝风险与妊娠相关限制)。
- 说明不同补充疗法证据强度有差异(如部分运动/行为方式证据更强,磁疗证据更有限),并使预期与已记录结局对齐。
- 在有用时组合兼容非药物方法(如环境调节 + 运动 + 放松),并复评哪种组合对个体患者反应最佳。
- 使用经皮神经电刺激(TENS)时按流程将电极置于目标神经通路附近;症状加重或出现禁忌担忧时应停止并升级。
- 在可用时考虑将生物反馈用于慢性疼痛,强调反复训练与就诊间自我调节技能迁移。
- 对非英语患者使用专业口译路径;发现障碍时使用药计划适配可负担性/可及性约束。
- 提供阿片使用、储存、处置及可能加重疼痛或降低方案效果的家庭因素的出院安全教育。
- 在首剂咨询与出院时纳入安全储药教学(置于儿童和访客无法触及/上锁位置)。
- 在临终舒适导向照护中,给药决策应优先与照护目标一致的症状缓解,而非仅依赖常规数字阈值拒绝用药。
- 在文化或灵性敏感的临终情境中,共同设计兼顾症状缓解与意识保持目标的方案(如滴定策略 + 非药物支持)。
- 在临终照护中应用“双重效应原则”:当意图是缓解痛苦时,即便可能出现非意图性镇静,按比例使用阿片在伦理上仍可支持。
- 慢性疼痛随访中,鼓励使用疼痛日志记录诱因、干预与功能反应,以指导与照护团队共同修订计划。
- 在儿科镇痛中,保持按体重给药并在给药前核验安全上限:
acetaminophen 10-15 mg/kg/dose q4-6h PRN,最大4 doses/day与80 mg/kg/day。ibuprofen 4-10 mg/kg/dose q6-8h PRN,最大400 mg/dose与40 mg/kg/day,上限1200 mg/day。
- 12 岁以下儿童及患水痘或流感样疾病的儿童/青少年避免使用阿司匹林(aspirin),以防 Reye 综合征风险。
- 对重度儿科疼痛,优先吗啡(morphine)或氢吗啡酮(hydromorphone)而非可待因(codeine)/曲马多(tramadol)(芬太尼(fentanyl)需更高谨慎),因代谢差异与呼吸风险顾虑。
阿片与 PCA 伤害风险
过度镇静通常先于呼吸抑制;早识别与纳洛酮就绪至关重要。
药理学
可行时采用“节阿片”策略,尤其在慢性疼痛与高风险人群。监测类别特异不良反应:非甾体抗炎药(NSAIDs) 的胃肠道(GI)出血/肾脏/心血管风险(如酮咯酸(ketorolac)等需短疗程谨慎)、过量对乙酰氨基酚(acetaminophen)或合并大量饮酒导致肝风险、以及阿片或镇静药组合导致中枢神经系统(CNS)抑制。区分耐受(反应减弱需更高剂量)、生理依赖(突然停药出现戒断)与成瘾(尽管有害仍强迫性使用),并持续执行严格安全监测。对辅助药物(如三环类、加巴喷丁类药物(gabapentinoids)、皮质激素、肌松药、局麻外用药),应纳入药物特异的精神/镇静/代谢监测及停药递减计划(若存在停药风险)。
临床判断应用
临床情景
一名术后使用 PCA 的患者报告突破痛持续且嗜睡加重。
- 识别线索:控制不足并伴镇静警示信号。
- 分析线索:当前 PCA 或辅助方案在疗效与安全之间可能失衡。
- 优先假设:即时优先项是在保持镇痛同时确保呼吸安全。
- 生成方案:复评 PCA 设置、复核并用镇静药、增加非阿片/非药物支持。
- 采取行动:升级至医师、加强监测并实施修订后的多模式方案。
- 评估结果:在疼痛-功能平衡改善的同时,警觉度更安全。
相关概念
- 全面疼痛评估与记录 - 提供安全滴定所需基线与复评数据。
- 疼痛通路、闸门控制与分类 - 多模式策略的机制学依据。
- 疼痛的生理、行为与情感反应 - 解读治疗反应信号与痛苦线索。
- 给药安全措施 - 用药流程防护与差错预防。
- 老年人疼痛 - 风险-获益平衡改变的人群背景。
自我检测
- 哪些发现提示“阿片毒性”而非“单纯疼痛未控”?
- 护士在每次交接必须核验哪三个 PCA 程序化要素?
- 为什么多模式治疗通常优于单药不断加量?