器官对体液与电解质的调节
关键要点
- 全身体液主要由肾脏系统调节。
- 肾脏反复循环约 5-6 升血液,在选择性重吸收前每日可形成约 200 升滤液。
- 当体液不足(低血容量)时,抗利尿激素(ADH)释放增加,促进肾脏水重吸收。
- 当肾小管液体容量较高时,ADH 被抑制,尿液更稀释。
- 血清渗透压正常约 275-295 mmol/kg,反映血液浓缩状态。
- Osmolality 指每千克溶剂中的溶质粒子数,osmolarity 指每升溶剂中的溶质粒子数。
- 尿比重正常约 1.010-1.020;数值升高提示浓缩,降低提示稀释。
- 口渴、中枢渗透压感受器、ADH 与 RAAS 共同协调血管内容量和血压。
- RAAS 可在低血压或低血清钠时被激活,增加血管张力并促进钠水潴留,同时促进钾排泄。
- 醛固酮是肾生理中钠钾处理的关键调节因子,通过钠重吸收支持水潴留。
- 稳定成人每日液体排出主要经肾脏(约 60%),其余为皮肤/胃肠道(GI)/肺不感蒸发损失(约 40%)。
- 心脏利钠肽在液体过负荷时通过促进血管扩张和钠水排泄来对抗 RAAS。
- 稳态控制通过“受体、控制中心、效应器”信号环纠正偏离设定点。
- 负反馈是主要稳态环路模式,通过逆转偏离来恢复正常范围。
- 正反馈会放大刺激以快速完成特定生物事件,必须及时终止以避免不稳定。
- 高渗和低渗状态若未及时纠正,均可引起严重神经系统恶化。
- 在感知、环路激活、反应执行或设定点调控任一环节失败,都可进展为细胞损伤和器官功能障碍。
- 电解质异常常相互依赖,一项严重紊乱可触发多电解质连锁反应。
病理生理学
体液和电解质稳态依赖器官系统与激素的相互作用,而非孤立实验室数值。肾脏调节总体体液,并通过 ADH 调节响应肾小管压力和容量状态。肾滤过依赖压力:肾小球毛细血管静水压支持滤液形成,肾灌注压低会减少废物与液体清除。
当体液丢失且血管内钠浓度上升时,血清渗透压增加。下丘脑渗透压感受器触发口渴并增加 ADH 释放,促进肾脏保水。该调节通路依赖可获得液体且能在口渴出现时饮水。
RAAS 在低压和低钠状态下也可支持灌注。血压下降或血清钠下降会刺激肾脏释放肾素。肾素将肝来源血管紧张素原转为血管紧张素 I,肺中的血管紧张素转换酶将其转为血管紧张素 II。血管紧张素 II 引起血管收缩并刺激醛固酮释放,增加肾钠重吸收使水回到血管内,同时增加钾排泄。
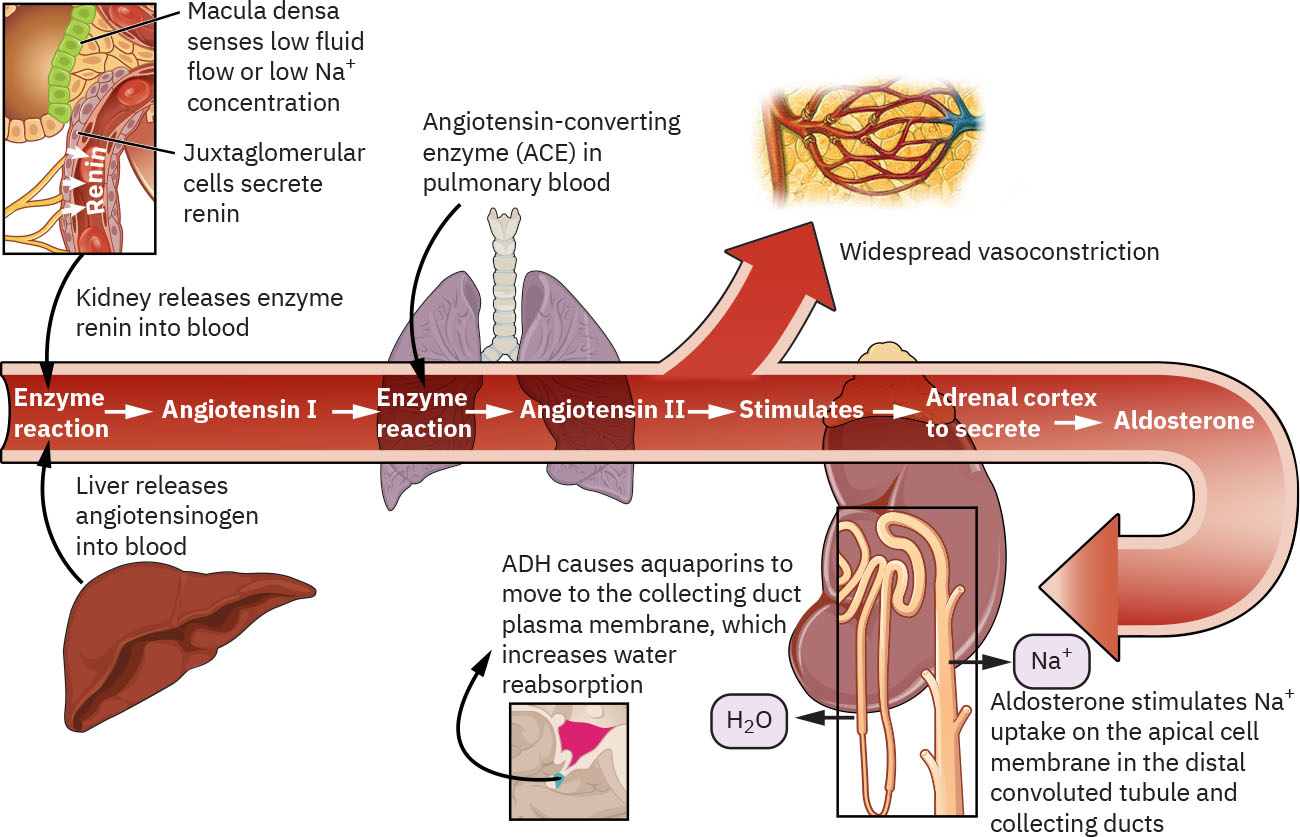 Illustration reference: OpenStax Clinical Nursing Skills Ch.19.1.
Illustration reference: OpenStax Clinical Nursing Skills Ch.19.1.
利钠肽在生理上与 RAAS 相对抗。当心脏组织感知液体过负荷和压力升高时,利钠肽促进血管扩张和肾脏排钠,以降低循环容量和压力。 除 ADH、RAAS 和利钠肽外,胰岛素、肾上腺素、糖皮质激素及甲状旁腺轴激素等内分泌因素也会影响特定电解质模式。 肾素释放部分由肾小球旁器调节,该结构邻近肾小球,将肾单位灌注感知与 RAAS 激活直接连接。
在摄入充足时,肾脏通常每日生成约 1,500 mL 尿液。少尿是体液不足与肾损伤路径中的早期预警信号,应结合情境进行趋势监测。
分类
- 保容量反应:低血容量时 ADH 增加,水重吸收增加。
- 排容量反应:肾小管液体容量高时 ADH 抑制,尿液稀释。
- 渗透压感受器-口渴反应:血清渗透压升高驱动口渴和 ADH 释放。
- 渗透压测量领域:osmolality 量化每 kg 溶剂粒子数;osmolarity 量化每 L 溶剂粒子数。
- 高渗模式:高溶质状态(如脱水或糖尿病相关状态),有循环应激与神经症状风险。
- 低渗模式:低溶质状态(如游离水过多或水平衡失调),有脑水肿和神经恶化风险。
- RAAS 恢复压力反应:肾素(Renin)激活后可经血管紧张素 II(angiotensin II)与醛固酮(aldosterone)通路增加血管张力与钠水潴留。
- RAAS 序列细节:肾素(Renin)与血管紧张素原(angiotensinogen,肝)作用生成血管紧张素 I(angiotensin I),再经 ACE(肺)转换为血管紧张素 II(angiotensin II)。
- 利钠肽反向调节:心脏肽在液体过负荷/高压时促进血管扩张和钠水排泄。
- 反馈环控制架构:受体检测、中央整合和效应器反应共同纠正体液/电解质偏离。
- 负反馈环模式:抑制性反应减少初始偏离,使变量回归设定点。
- 正反馈环模式:放大反应增加初始刺激直至终点完成(如凝血、泌乳反射和分娩子宫收缩)。
- 稳态失败模式:检测失败、反馈启动失败、效应器反应失败、设定点失调。
- 钠调节通路:肾脏系统,受醛固酮影响。
- 钾调节通路:肾脏系统,受醛固酮并联胰岛素、肾上腺素和糖皮质激素影响。
- 钙调节通路:骨骼-内分泌交互,涉及甲状旁腺激素、维生素 D 和降钙素。
护理评估
NCLEX 重点
先将症状与最可能受调节的电解质通路匹配,再用化验与容量趋势验证。
- 追踪出入量、尿液浓缩模式和净体液平衡,以识别 ADH 相关容量线索。
- 当稀释或浓缩状态不清时,联合趋势监测血清渗透压与尿渗透压/尿比重模式。
- 评估功能性障碍(认知改变、无力、液体获取差)是否限制对口渴线索的反应。
- 评估低灌注代偿模式(如低血压伴心动过速),这可先于肾滤过恶化出现。
- 对钠平衡紊乱,评估意识混乱、易激惹、口渴、黏膜干燥、头痛、癫痫风险和昏迷进展。
- 对钾平衡紊乱,评估胃肠绞痛、无力、脉搏质量和心电图(ECG)改变,包括 T 波高尖或低平/倒置及 U 波模式。
- 对钙平衡紊乱,评估胃肠症状、肌无力、刺痛、痉挛和手足搐搦。
- 升级低尿量趋势,包括持续 8 小时尿量 <30 mL/小时(或 <0.5 mL/kg/小时)。
- 将症状模式与连续生化值和临床轨迹相关联。
- 当液体潴留加重但尿量下降时,考虑混合模式:血清更稀释而尿液仍相对浓缩。
护理干预
- 当容量或神经趋势提示代偿调节失效时,优先早期干预。
- 协调连续化验与聚焦再评估,判断器官层调节是否正在恢复平衡。
- 执行已下达液体策略,并监测尿液反应是否符合预期 ADH 相关效应。
- 对照成人预期水平衡范围(稳定状态约摄入 2,500 mL、排出 2,500 mL)监测每日出入量模式。
- 对慢性肾脏与内分泌风险患者强化钠和钾管理教育。
- 当心电图(ECG)或神经表现提示严重电解质不稳定时快速升级。
代偿极限
器官-激素代偿在急性状态具有保护作用,但在慢性病或重度失衡中无法完全阻止恶化。
药理学
| 药物类别 | 示例 | 关键护理注意事项 |
|---|---|---|
| [diuretics] | 袢利尿剂与保钾类 | 利尿剂会改变钠、钾和体液平衡,需密切趋势监测。 |
| [intravenous-fluid-categories-tonicity-and-infusion-regulation](电解质替代治疗) | 钠或钾补充方案 | 纠正必须由连续化验、肾脏状态和症状严重度共同指导。 |
临床判断应用
临床情景
一名慢性肾病患者出现液体潴留、电解质异常和逐渐出现的神经系统症状。
- 识别线索: 体液平衡异常、尿液模式改变,以及令人担忧的钠/钾症状谱。
- 分析线索: 肾脏-内分泌调节未能维持稳态。
- 确定优先假设: 即时风险包括神经功能下降和心脏传导不稳定。
- 提出解决方案: 强化监测、获取连续化验/心电图(ECG),并执行已下达容量-电解质纠正。
- 采取行动: 升级恶化并实施病因导向管理。
- 评估结局: 尿量、化验和症状向稳定基线回归。
相关概念
- 钠平衡紊乱 - 钠表现可映射为肾-醛固酮调节失效或过负荷状态。
- 钾平衡紊乱 - 钾不稳定反映肾处理及激素调节转移。
- 体液容量不足、低血容量与脱水 - 低容量状态驱动 ADH 介导保水。
- 体液容量过多(高容量) - 高容量状态可伴 ADH 抑制和稀释模式。
- 肾脏疾病 - 慢性肾功能障碍会降低维持体液-电解质稳态能力。
自我检查
- 在低血容量与高肾小管液体容量状态下,ADH 行为有何不同?
- 哪些症状簇提示钠、钾或钙失调?
- 为什么慢性肾病患者即使激素通路被激活,代偿仍可能失败?