Manejo multimodal del dolor y seguridad de PCA
Puntos clave
- El manejo multimodal del dolor combina medicamentos e intervenciones no farmacologicas para mejores resultados.
- La terapia opioide requiere monitoreo estricto de sedacion, depresion respiratoria, dependencia y riesgo de sobredosis.
- Las terapias no opioides y coadyuvantes amplian el control mientras reducen la carga de opioides.
- La PCA es efectiva cuando se siguen seleccion de pacientes, programacion de bomba, verificacion dual y protocolos de reevaluacion.
Fisiopatologia
El dolor esta mediado biologica, psicologica y socialmente; el tratamiento de modalidad unica suele dejar carga residual. La estrategia multimodal apunta a multiples mecanismos de forma simultanea, mejorando alivio y limitando toxicidad por escalamiento de dosis en una sola clase.
Los opioides reducen senalizacion del dolor pero pueden suprimir impulso respiratorio y cognicion. AINEs y acetaminofen apuntan a vias inflamatorias y nociceptivas, mientras coadyuvantes apoyan estados de dolor neuropatico, espastico o localizado.
Las intervenciones no farmacologicas (terapia de movimiento, imagen guiada, masaje, modulacion ambiental, estrategias cognitivas) reducen amplificacion central y mejoran funcion, afrontamiento y calidad de vida.
Cuando el dolor posoperatorio esta pobremente controlado, la senalizacion de hormonas de estres (por ejemplo exceso de cortisol), tendencia a hiperglucemia, persistencia inflamatoria y movilidad reducida pueden enlentecer curacion tisular y progreso de rehabilitacion mientras aumenta riesgo de complicaciones.
Clasificacion
- Nucleo farmacologico: Capas analgesicas opioide, no opioide y coadyuvante.
- Nucleo no farmacologico: Intervenciones fisicas, psicologicas, emocionales y ambientales.
- Contexto de escalera por severidad: Categorias de dolor leve/moderado/severo pueden guiar escalamiento paso a paso de medicamentos.
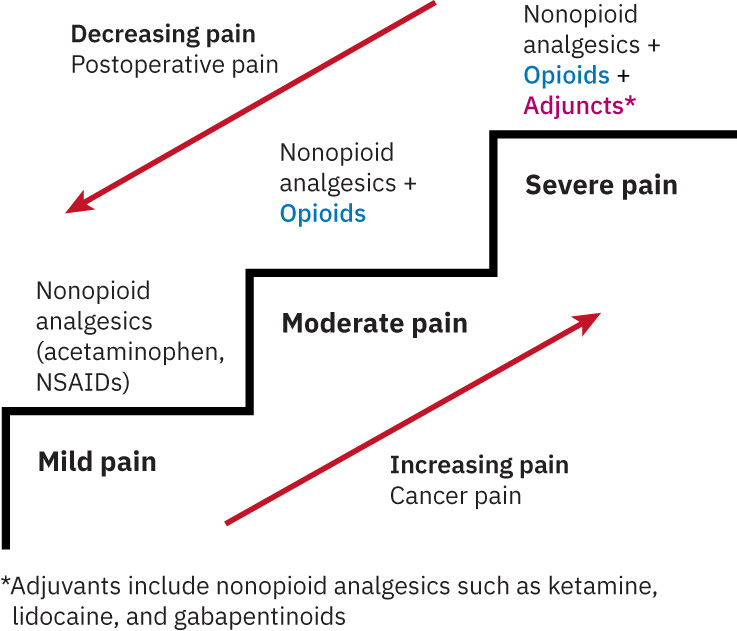 Illustration reference: OpenStax Medical-Surgical Nursing Ch.7.3.
Illustration reference: OpenStax Medical-Surgical Nursing Ch.7.3.
- Estructura PCA: Dosis de carga, dosis de demanda (bolo), tasa basal (si se usa), intervalo de bloqueo y limite maximo por una hora.
- Dominios de seguridad: Seleccion de candidatos, monitoreo, prevencion de eventos adversos e integridad de documentacion.
- Dominios de estandares de cuidado: Tamizaje de dolor en admision/ED, reevaluacion apropiada por edad/condicion, seguimiento de metas funcionales y educacion al alta sobre riesgo opioide.
Valoracion de enfermeria
Enfoque NCLEX
Evalua exito del tratamiento por tendencias de funcion y seguridad, no solo por intensidad analgesica.
- Evalua mecanismo del dolor y patron de severidad para seleccionar mezcla de clases de medicamentos.
- En ambitos hospitalarios, asegura que el dolor sea tamizado en admision (y en ingreso a ED cuando aplique) y reevaluado con herramientas ajustadas a edad, cognicion y capacidad de comunicacion.
- Escala de inmediato ante dolor severo nuevo o dolor no responsivo al plan actual; dolor severo subdito o dolor/presion toracica requiere respuesta inmediata a nivel de emergencia segun protocolo.
- Trata dolor irruptivo severo persistente pese a terapia activa para dolor cronico como indicio de escalamiento de mayor agudeza que puede requerir manejo intrahospitalario avanzado.
- Caracteriza patron detonante de dolor irruptivo (por ejemplo actividad, brote por estres/enfermedad, fallo al final de dosis o episodio no provocado) para decidir si el tratamiento solo de rescate es suficiente o se requiere revision de regimen basal.
- Evalua factores de riesgo opioide: vulnerabilidad a sedacion, riesgo de compromiso respiratorio, uso sedante concurrente.
- Evalua perfil de riesgo no opioide antes de seleccionar (por ejemplo estado de adulto mayor, embarazo y contexto de comorbilidad hepatica/cardiovascular/renal/GI).
- Evalua candidatura para PCA: cognicion, capacidad de seguir indicaciones y perfil de contraindicaciones.
- Evalua explicitamente perfil de contraindicaciones de PCA (por ejemplo alergia a opioides, preocupacion de infeccion activa, presion intracraneal elevada, disfuncion renal severa o contexto de riesgo de sangrado) segun politica institucional.
- Trata confusion o sobresedacion como indicios de exclusion para PCA porque el uso seguro de PCA requiere activacion del boton por el propio paciente en estado de alerta.
- Evalua ideas equivocadas sobre opioides (por ejemplo temor de adiccion durante uso posquirurgico a corto plazo) que reducen adherencia a planes analgesicos.
- En rutas posoperatorias, refuerza que el uso opioide a corto plazo para dolor quirurgico agudo es distinto al trastorno por uso de sustancias, aun aplicando monitoreo de seguridad estandar.
- En pacientes con antecedente conocido de trastorno por uso de sustancias, anticipa posible mayor requerimiento opioide posoperatorio por tolerancia y escala en colaboracion para dosificacion individualizada.
- Para uso opioide en atencion primaria de adultos, evalua alineacion del plan con dominios CDC de prescripcion: necesidad de inicio, seleccion/dosis de opioide, duracion inicial con seguimiento y mitigacion de dano-riesgo.
- Antes de prescribir opioides ambulatorios o continuar terapia, verifica historial de sustancias controladas en PDMP; cuando la terapia opioide cronica continua, repite revision PDMP al menos cada 3 meses segun alineacion de politica/guia.
- Evalua respuesta a terapias no farmacologicas y barreras de adherencia del paciente.
- Evalua si modalidades no farmacologicas seleccionadas se usan como terapia complementaria (con medicamentos) o terapia alternativa (en lugar de medicamentos), y verifica ajuste de seguridad/meta para cada via.
- Evalua todo uso actual de productos naturales (hierbas, vitaminas, suplementos, aceites) y posible riesgo de interaccion; recuerda a pacientes que muchos suplementos no estan regulados por FDA para seguridad/efectividad de la misma manera que medicamentos de prescripcion.
- Evalua elegibilidad para modalidades electricas (por ejemplo TENS) tamizando estado de dispositivo implantable y contextos de contraindicacion mayor (por ejemplo restricciones especificas de embarazo, sangrado activo/hemorragia, trastorno convulsivo, cancer o riesgo de DVT).
- Evalua riesgo de subtratamiento en poblaciones no verbales, con deterioro cognitivo, con supresion cultural del dolor y con barrera idiomatica.
- Evalua creencias del paciente sobre significado del dolor, tratamientos aceptables y remedios tradicionales para prevenir subreporte o rechazo guiado por cultura.
- Evalua patrones de amplificacion por temor (por ejemplo algofobia, catastrofizacion o conducta de evitacion) que pueden aumentar dolor percibido y reducir funcion.
- Evalua contexto de trauma y PTSD cuando dolor esta vinculado a lesion o abuso pasado, porque trauma no tratado puede sostener ciclos de distrs por dolor.
- Evalua afrontamiento maladaptativo (por ejemplo automedicacion con alcohol/sustancias, retiro severo de actividad) y habitos protectores (movimiento, rutina de sueno, regulacion de estres).
- Evalua conductas aprendidas de dolor (por ejemplo inactividad prolongada porque da alivio de corto plazo) que pueden empeorar dolor y funcion a largo plazo.
- Evalua si preservar conciencia/estado de alerta es prioridad en enfermedad seria o cuidado de fin de vida, porque esto puede afectar aceptacion de analgesicos sedantes.
- Evalua barreras practicas de acceso (por ejemplo disponibilidad de interprete, costo/cobertura de medicacion y acceso a seguimiento) que pueden reducir efectividad del plan de dolor.
Intervenciones de enfermeria
- Implementa pasos de seguridad en medicacion: paciente/medicamento/dosis/via/tiempo correctos mas vigilancia posdosis.
- Documenta analgesicos administrados de inmediato en MAR/eMAR y actualiza prontamente registros de intervenciones no farmacologicas para reducir riesgo de dosis duplicada y error en relevo.
- Para sesiones planificadas de rehabilitacion, coordina momento de premedicacion interdisciplinaria (comunmente 30-60 minutos antes de PT/OT) para mejorar participacion y seguridad.
- Completa reevaluacion de dolor antes y despues de administracion analgesica para confirmar indicacion y respuesta.
- Si hay nausea/vomito, coordina con el prescriptor para usar la via mas efectiva y evitar dosificacion oral cuando absorcion/tolerancia oral sea no confiable.
- Minimiza distracciones durante preparacion/administracion de opioides y sigue procesos de doble verificacion independiente para manejo de alto riesgo segun politica.
- Sigue politica de descarte de sustancias controladas con documentacion de testigo requerida cuando ocurre descarte de opioides.
- Combina tratamiento farmacologico con al menos una modalidad no farmacologica cuando sea factible.
- Para lesion aguda de tejido blando, inicia temprano patron RICE (reposo, hielo, compresion, elevacion) y reevaluar progresion despues de las primeras 24-48 horas cuando metas cambian de control de inflamacion a curacion tisular y restauracion de movilidad.
- Usa termoterapia de forma deliberada: calor comunmente cerca de 5-20 minutos para rigidez/molestia cronica y frio hasta 20 minutos para inflamacion aguda; manten barrera entre piel y fuente de calor/frio e inspecciona piel de forma rutinaria por lesion.
- Evita supuestos basados en estereotipos (por ejemplo “cultura estoica significa no dolor”); combina autorreporte, conducta y hallazgos clinicos para planes individualizados.
- Selecciona modalidades no farmacologicas alineadas con preferencia y metas del paciente (por ejemplo distraccion, relajacion, posicionamiento, estimulacion cutanea o enfoques mente-cuerpo), y documenta efectividad frente a metas de confort.
- En ambitos intrahospitalarios, confirma requisitos de orden del proveedor antes de aplicar modalidades no farmacologicas como calor/frio, masaje, acupuntura/acupresion y vias basadas en TENS.
- Enmarca pruebas no farmacologicas como iterativas e individualizadas: si una modalidad es segura pero inefectiva, cambia de metodo en lugar de abandonar por completo el cuidado no farmacologico.
- Combina planes de dolor cronico con estrategias de afrontamiento CBT/mindfulness y enfoques de exposicion gradual/actividad gradual cuando existe evitacion por miedo.
- Usa opciones practicas basadas en movimiento (fisioterapia, ejercicio de baja intensidad o movimiento/respiracion estilo yoga) para mejorar movilidad, regulacion de estres y funcion.
- Ofrece coadyuvantes naturales y mente-cuerpo seleccionados cuando sea apropiado (por ejemplo aromaterapia, imagen guiada, meditacion, mindfulness, CBT o movimiento estilo yoga/tai-chi), y documenta beneficio versus carga especifica del paciente.
- Usa opciones de distraccion de apoyo creativo/con animales cuando esten disponibles (por ejemplo arte, musica o vias de terapia con mascotas) para mejorar relajacion y reducir saliencia de senal de dolor.
- Para dolor cronico con patron inflamatorio (por ejemplo contextos de fibromialgia), refuerza consejeria dietaria que enfatiza vegetales, granos integrales y proteinas magras mientras reduce azucares refinados y exceso de carne roja cuando se alinea con metas nutricionales.
- Brinda ensenanza de medicacion en lenguaje culturalmente sensible y linguisticamente apropiado, usando visuales/demostracion cuando sea necesario para ajuste de alfabetizacion en salud.
- Refuerza que el manejo del dolor es un derecho del paciente y que el tratamiento temprano es mas seguro que esperar escalamiento severo.
- En coexistencia de SUD y dolor, enmarca planificacion alrededor de dos metas paralelas: tratar dolor adecuadamente mientras se aborda riesgo SUD con salvaguardas estructuradas.
- Entrena a pacientes que evitar dolor y no reportarlo puede demorar diagnostico/tratamiento de causas serias; refuerza reporte temprano y reevaluacion oportuna.
- Construye planes de dolor con paciente/familia usando metas realistas y medibles que incluyan funcion (por ejemplo respirar, girar, deambular), no solo objetivos de puntaje.
- Usa metas funcionales pequenas y alcanzables para contrarrestar desesperanza y reforzar senales de eficacia del tratamiento con el tiempo.
- Ajusta intensidad y via analgesica a severidad reportada usando enfoque escalonado (primero no opioide cuando sea apropiado, luego escalar), favoreciendo la dosis efectiva mas baja con la via menos invasiva.
- En trayectorias de dolor agudo severo, ensena pasos esperados de transicion (por ejemplo opioide IV a opioide oral a no opioide conforme mejora la condicion) para que los pacientes anticipen cambios de descenso.
- En planificacion de alta posoperatoria, transiciona analgesia de via IV a via oral cuando recuperacion se estabiliza; evita dosificacion de opioide IV de ultimo minuto justo antes del alta porque aun se requiere monitoreo respiratorio.
- Aplica logica de escalera WHO con flexibilidad: el dolor agudo severo puede requerir iniciar en un peldano de mayor potencia con descenso posterior, mientras dolor cronico suele escalarse paso a paso desde peldanos bajos.
- En dolor cronico no oncologico, evita estrategias de opioide de primera linea de rutina cuando existan alternativas efectivas; usa opioides solo despues de revision riesgo-beneficio y plan de monitoreo.
- Para dolor asociado a OUD, maximiza primero opciones no farmacologicas y no opioides (por ejemplo ejercicio/fisioterapia/CBT, AINEs, agentes topicos y coadyuvantes seleccionados como SNRIs/TCAs); si opioides son clinicamente necesarios, no retenerlos solo por antecedente de OUD.
- En pacientes menores de 18 anios, evita estrategias de dolor de primera linea con opioides cuando existan alternativas efectivas; si se requieren opioides, usa la dosis efectiva mas baja con monitoreo intensificado.
- Para analgesicos PRN, verifica dosis administradas en las 24 horas previas y limites acumulativos antes de dar una dosis adicional.
- Para rangos PRN ambulatorios (por ejemplo una a dos tabletas), ensena “inicia bajo y luego reevaluar” para evitar sobresedacion o sobredosis innecesarias.
- Cuando se requiere terapia opioide en pacientes con riesgo SUD, establece metas compartidas/riesgos conocidos, usa acuerdo de tratamiento, inicia bajo y titula lento, y programa reevaluacion de seguimiento cercano.
- Para PCA, verifica ajustes de bolo/basal/bloqueo con firma dual de enfermeria segun politica.
- En pediatria, usa PCA solo cuando el ninio es capaz en desarrollo/cognicion (comunmente edad >6 anios con comprension adecuada) y refuerza activacion del boton solo por el paciente.
- Educa paciente/familia que solo el paciente debe activar PCA salvo que protocolo explicito diga lo contrario.
- Intensifica monitoreo PCA para perfiles de alto riesgo (por ejemplo apnea del sueno, obesidad, deterioro renal/hepatico o exposicion reciente a sedacion/anestesia).
- Mantiene acceso inmediato a naloxona cuando terapia opioide esta activa y trata sobresedacion como advertencia temprana de depresion respiratoria inminente.
- Intensifica controles de sedacion/respiracion para pacientes naive a opioides, aumentos recientes de dosis opioide o exposicion concurrente a benzodiazepina/sedante.
- Monitoriza eventos adversos comunes de opioides/PCA (por ejemplo estrenimiento, nausea/vomito, prurito, retencion urinaria) y trata temprano para sostener adherencia.
- Anticipa temprano ordenes para manejo de eventos adversos de opioides (por ejemplo ablandador/laxante y antiemetico) para reducir interrupcion del tratamiento.
- Reevalua efecto analgesico por via e inicio (comunmente cerca de 15-30 minutos despues de IV y dentro de cerca de 60 minutos despues de dosis oral, segun politica); si dolor sigue sobre nivel aceptable, escala opciones farmacologicas y no farmacologicas y notifica al proveedor.
- Si episodios irruptivos recurren pese a dosificacion de rescate, escala para revision de plan (por ejemplo ajuste de regimen basal mas apoyo no farmacologico dirigido a detonantes) en lugar de repetir ciclos solo de rescate.
- Para administracion opioide neuraxial/implantada (por ejemplo bombas epidural o intratecal), monitoriza de cerca por complicaciones de dosis/dispositivo y escala de inmediato ante signos de abstinencia, cambio neurologico o deterioro cardiorrespiratorio.
- En relevo, reconcilia conteos de demanda versus administrado y volumen restante de sustancia controlada con documentacion de enfermeria dual.
- Monitoriza funcion intestinal e inicia medidas de prevencion (liquidos, deambulacion temprana, plan ablandador/laxante) cuando existe riesgo de estrenimiento inducido por opioides.
- Para casos complejos de dolor o riesgo opioide, escala rutas de derivacion (por ejemplo especialista en dolor o apoyo para tratamiento opioide) segun politica.
- Para carga de dolor vinculada a trauma, coordina rutas de derivacion de salud mental informada en trauma junto con cuidado analgesico.
- Inicia proactivamente estrategias de prevencion intestinal por opioides (hidratacion, fibra/dieta segun corresponda, plan ablandador/laxante, movilidad) salvo contraindicacion.
- Usa apoyos ambientales no farmacologicos (optimizacion de luz/ruido/temperatura) con relajacion, respiracion, CBT y enfoques basados en movimiento.
- Agrupa tareas de cuidado cuando sea factible para reducir interrupcion del sueno y preservar descanso restaurador durante periodos de recuperacion dolorosa.
- Usa estrategias de distraccion (musica, conversacion, juegos, actividades guiadas) alrededor de procedimientos y brotes diarios; pacientes pediatricos suelen responder fuerte a distraccion apropiada para su edad.
- Tamiza contraindicaciones antes de opciones de toque terapeutico (por ejemplo rash/infeccion activa, estados de riesgo cardiovascular seleccionados, precauciones especificas de embarazo) e individualiza presion/intensidad.
- Usa masaje/manipulacion solo cuando tamizaje de riesgo sea aceptable; evita o escala revision en pacientes anticoagulados y en contextos como fractura, riesgo de coagulo, herida abierta/infeccion o fragilidad osea.
- Para rutas de acupuntura, confirma prestacion por proveedor entrenado y tamizaje de contraindicaciones (por ejemplo contexto de marcapasos, riesgo por anticoagulacion y restricciones relacionadas con embarazo) antes de derivar.
- Explica que la fuerza de evidencia difiere entre modalidades complementarias (por ejemplo mas fuerte para enfoques seleccionados de movimiento/conducta, mas limitada para afirmaciones de terapia magnetica) y alinea expectativas con resultados documentados.
- Combina metodos no farmacologicos compatibles cuando sea util (por ejemplo ajuste ambiental mas movimiento mas relajacion) y reevaluar que mezcla de componentes produce la mejor respuesta especifica del paciente.
- Para uso TENS, coloca electrodos cerca de vias nerviosas objetivo segun protocolo y detener/escalar si sintomas empeoran o emergen preocupaciones de contraindicacion.
- Considera biofeedback para dolor cronico cuando este disponible, enfatizando sesiones repetidas de entrenamiento y transferencia de habilidades de autorregulacion entre visitas.
- Usa rutas de interprete profesional para pacientes no angloparlantes y adapta planes de medicacion a restricciones de asequibilidad/acceso cuando se identifiquen barreras.
- Apoya ensenanza de seguridad al alta para uso, almacenamiento y desecho de opioides, mas factores del hogar que puedan empeorar dolor o reducir efectividad del plan.
- Incluye ensenanza de almacenamiento seguro de medicamentos (mantener fuera de alcance/bajo llave lejos de ninos y visitantes) en consejeria de primera dosis y al alta.
- En cuidado enfocado en confort de fin de vida, decisiones de dosis priorizan alivio sintomatico alineado con metas de cuidado en lugar de umbrales numericos rutinarios de retencion por si solos.
- En contextos de fin de vida cultural o espiritualmente sensibles, co-disena planes que equilibren alivio de sintomas con metas de conciencia (por ejemplo estrategia de titulacion mas apoyo no farmacologico).
- Aplica la regla de doble efecto en fin de vida: cuando la accion intencionada es aliviar sufrimiento, el uso opioide proporcional esta eticamente respaldado incluso si puede ocurrir sedacion no intencionada.
- Para seguimiento de dolor cronico, anima diario de dolor que registre detonantes, intervenciones y respuesta funcional para guiar revision del plan con el equipo de cuidado.
- En analgesia pediatrica, mantiene dosificacion basada en peso y verifica limites seguros antes de administrar:
acetaminophen 10-15 mg/kg/dose q4-6h PRN, máximo4 doses/dayy80 mg/kg/day.ibuprofen 4-10 mg/kg/dose q6-8h PRN, máximo400 mg/dosey40 mg/kg/dayhasta1200 mg/day.
- Evita aspirina en ninos menores de 12 anios y en ninos/adolescentes con varicela o enfermedad tipo influenza por riesgo de sindrome de Reye.
- Para dolor pediatrico severo, prefiere morfina o hidromorfona sobre codeina/tramadol (y usa fentanyl con cautela aumentada) por metabolismo variable y preocupaciones de riesgo respiratorio.
Riesgo de dano por opioides y PCA
La sobresedacion suele preceder depresion respiratoria; reconocimiento temprano y preparacion con naloxona son criticos.
Farmacologia
Usa estrategias ahorradoras de opioides cuando sea posible, especialmente en dolor cronico y poblaciones de alto riesgo. Monitoriza eventos adversos especificos por clase: riesgo GI/renal/cardiovascular con AINEs (con precaucion de corta duracion para agentes como ketorolac), riesgo hepatico con exceso de acetaminofen o uso concurrente importante de alcohol, y depresion del SNC con combinaciones de opioides o sedantes. Diferencia tolerancia (respuesta reducida que requiere dosis mayor), dependencia fisica (abstinencia con suspension abrupta) y adiccion (uso compulsivo pese a dano), manteniendo monitoreo estricto de seguridad. Para opciones coadyuvantes (por ejemplo triciclicos, gabapentinoides, corticosteroides, relajantes musculares, anestesicos topicos), incluye monitoreo psiquiatrico/sedacion/metabolico especifico por agente y planes de descenso cuando exista riesgo de suspension.
Aplicacion del juicio clinico
Escenario clinico
Un paciente posquirurgico en PCA reporta dolor irruptivo persistente y somnolencia creciente.
- Reconocer indicios: Control inadecuado mas signos de advertencia por sedacion.
- Analizar indicios: El plan actual de PCA o coadyuvantes puede estar desbalanceado entre eficacia y seguridad.
- Priorizar hipotesis: La prioridad inmediata es seguridad respiratoria mientras se preserva analgesia.
- Generar soluciones: Reevalua ajustes PCA, revisa sedantes concurrentes, agrega apoyo no opioide/no farmacologico.
- Actuar: Escala al proveedor, intensifica monitoreo e implementa plan multimodal revisado.
- Evaluar resultados: Perfil de alerta mas seguro con mejor balance dolor-funcion.
Conceptos relacionados
- valoracion integral del dolor y documentacion - Aporta datos de linea basal y reevaluacion requeridos para titulacion segura.
- via del dolor control de compuerta y clasificacion - Fundamentacion por mecanismo para enfoque multimodal.
- respuestas fisiologicas conductuales y afectivas al dolor - Interpreta senales de respuesta a tratamiento e indicios de distrs.
- medidas de seguridad en administracion de medicamentos - Salvaguardas del proceso de medicacion y prevencion de errores.
- dolor en adultos mayores - Contexto poblacional para balance riesgo-beneficio alterado.
Autoevaluacion
- Que hallazgos sugieren toxicidad opioide en lugar de solo dolor no controlado?
- Que tres elementos programados de PCA debe verificar enfermeria en cada relevo?
- Por que la terapia multimodal suele superar el escalamiento de agente unico?