止血、凝血與纖維蛋白溶解
重點整理
- 脾臟與肝臟是血球處理與凝血調控的重要輔助器官。
- 止血依序經過血管痙攣、血小板血栓形成,以及纖維蛋白穩定化的凝血階段。
- 纖維蛋白溶解透過活化 plasmin 分解纖維蛋白並恢復血流,以限制血栓負荷。
- Warfarin 透過拮抗維生素 K 減緩凝血因子活化,需常規 INR 監測。
- 凝血缺陷可使用血液成分治療:FFP 用於凝血因子補充,冷凍沉澱用於纖維蛋白原相關疾病。
病理生理學
血液生理由骨髓造血、輔助器官與協調性凝血控制共同支持。於骨髓中,erythropoietin 驅動之紅血球生成仰賴足夠的鐵、維生素 B12、葉酸、銅與鈷。thrombopoietin 調控血小板生成,少部分血小板儲存在脾臟,多數則在血液循環。脾臟負責儲存與過濾血液成分,白髓支持白血球活動,紅髓則作為紅血球與血小板儲庫。肝臟提供凝血酶原與其他凝血因子,並代謝血紅素分解產生的膽紅素。肝臟膽紅素處理受損可導致黃疸。
止血始於血管受損後,並以連結的階段進行。首先,局部血管平滑肌收縮以減少失血(血管痙攣)。接著,血小板黏附於暴露膠原、活化並聚集,形成暫時性血小板栓。之後凝血瀑布活化凝血因子,產生 thrombin,並將 fibrinogen 轉為 fibrin。交聯 fibrin 強化血小板栓,隨後血塊回縮使血塊更緻密,以支持傷口閉合。
凝血常分為外在途徑、內在途徑與共同途徑。外在(組織因子)途徑通常較快,組織受損後數秒內即可完成;內在途徑較複雜,通常於數分鐘內發展。兩者皆於共同途徑的 Factor X 活化處匯流,隨後將 prothrombin(Factor II)轉為 thrombin、fibrinogen(Factor I)轉為 fibrin,並由 Factor XIII 穩定血塊。
纖維蛋白溶解透過將 plasminogen 活化為 plasmin 來平衡血塊形成,常由 tissue plasminogen activator(tPA)促成。plasmin 會將 fibrin 分解為較小產物,縮小血塊並協助恢復血流。調控失衡會使風險偏向血栓或出血。
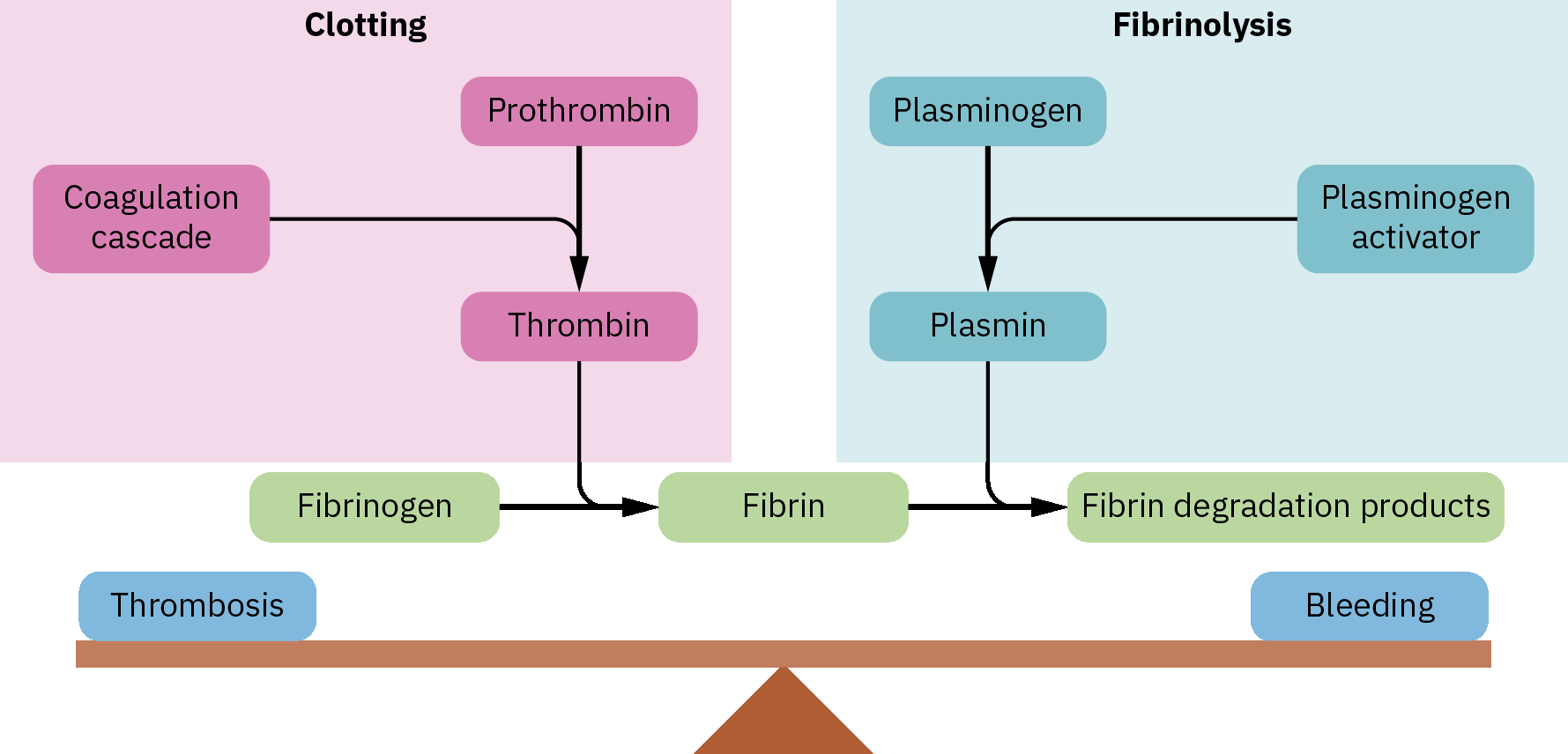 Illustration reference: OpenStax Pharmacology Ch.20.1.
Illustration reference: OpenStax Pharmacology Ch.20.1.
生理性抗凝機制可限制血塊向受傷部位外延伸。antithrombin 會抑制 Factor X 活性與 thrombin 生成,而內源性 heparin(由嗜鹼性球與肥大細胞路徑釋放)可支持此抗凝效果。若血栓形成於完整或僅輕度受損的血管中,可能部分阻斷血流,或於小血管造成完全阻塞。
臨床上,血栓性與出血性疾病可歸納為血管型、血小板型與凝血型異常。血管異常會改變管腔血流並促進鬱滯相關凝血;血小板數量/品質缺陷會影響初級止血;維生素 K 缺乏或肝功能障礙可造成凝血路徑失敗。後天性疾病如彌散性血管內凝血可同時出現凝血因子耗竭、微血栓與出血風險。
分類
- 初級止血:血管痙攣與血小板黏附/活化/聚集。
- 次級止血:外在與內在瀑布活化,於共同途徑匯流生成 thrombin 與 fibrin。
- 血塊清除:透過 plasmin 介導 fibrin 降解的纖維蛋白溶解。
- 疾病型態框架:血管、血小板與凝血/纖維蛋白溶解異常可同時存在,且可在血栓與出血表現間快速轉換。
護理評估
NCLEX 焦點
優先辨識早期出血與血栓風險,並識別不安全的抗凝強度。
- 評估活動性出血線索(牙齦出血、流鼻血、黑便、血尿、穿刺點滲血)。
- 評估可能血栓線索(新發單側腫脹、胸痛、急性神經功能缺損)。
- 評估反覆或無誘因靜脈血栓栓塞型態與家族史,可能提示遺傳性易栓症。
- 回顧使用 warfarin 個案的凝血相關實驗室趨勢與 INR 值。
- 使用基線凝血參考值做趨勢判讀:INR 約 0.8-1.2、PT 約 11-13 秒、aPTT 約 25-35 秒(依實驗室而異)。
- 在抗凝監測情境下,預期治療性延長目標(例如 warfarin 的 INR 2-3,且有醫囑時 PTT/aPTT 約為基線 1.5-2 倍)。
- 將肝功能異常徵象(例如黃疸)與可能的凝血因子或膽紅素處理效應連結判讀。
- 凝血不穩定時,回顧營養與用藥史以辨識維生素 K 缺乏風險或維生素 K 拮抗作用。
- 在脾臟外傷情境中,緊急評估出血風險並準備快速診斷升級;脾切除後提高感染監測警覺。
護理介入
- 對疑似出血或血栓立即升級處置,因兩者皆可快速惡化。
- 凝血狀態不穩定時落實出血預防,並避免不必要侵入性處置。
- 強化 warfarin 安全:維持一致飲食維生素 K 型態、治療依從性與規律 INR 追蹤。
- 支持急性血栓事件的流程化應對,包含快速團隊溝通。
- 具適應症時協調凝血因子替代輸血流程(例如凝血因子流失/INR 升高情境使用 FFP;纖維蛋白原缺乏狀態如 dysfibrinogenemia 或 hypofibrinogenemia 使用冷凍沉澱)。
抗凝安全風險
抗凝過度會增加出血風險,而抗凝不足則會放任破壞性血栓形成。
藥理學
| 藥物類別 | 範例 | 關鍵護理考量 |
|---|---|---|
| anticoagulants | warfarin | 監測 INR 趨勢與出血風險;維持穩定維生素 K 攝取型態;理解 VKOR 抑制為核心機轉。 |
| thrombolytics | thrombolytics (tissue-plasminogen-activator) | 用於特定急性阻塞事件;需密切監測出血併發症。 |
臨床判斷應用
臨床情境
一位使用 warfarin 的個案在常規追蹤中出現自發性牙齦出血,且 INR 高於目標。
- 辨識線索(Recognize Cues):新發出血徵象加上抗凝超治療指標。
- 分析線索(Analyze Cues):凝血受到過度抑制,近期出血風險升高。
- 排序假設(Prioritize Hypotheses):最高優先是抗凝相關出血併發症。
- 提出解決方案(Generate Solutions):依流程暫停/升級處置、加強監測,並回顧用藥/飲食因素。
- 採取行動(Take Action):執行出血預防並通知醫師目前發現。
- 評估結果(Evaluate Outcomes):出血緩解且 INR 回到治療範圍。
關聯概念
- 免疫系統 - 脾臟白髓連結免疫與血液功能。
- ABO 血型相容性與輸血安全 - 血液製品安全與凝血風險狀態相互關聯。
- 輸血核對、啟動與反應處置 - 血液相關不穩定狀態的程序層級應對。
- 傷口癒合階段與閉合意圖 - 止血是組織修復第一階段。
- 血友病 - 遺傳性因子缺乏是高價值出血疾病應用範例。
- 骨髓衰竭與血球低下型態可改變出血與感染脆弱性。
自我檢核
- 初級止血、次級止血與纖維蛋白溶解在臨床上的目的分別為何?
- 為何 warfarin 治療需要 INR 監測與穩定維生素 K 攝取型態?
- 哪些評估發現提示抗凝相關惡化且需緊急處置?