类风湿关节炎:自身免疫性关节疾病
要点
- 类风湿关节炎(rheumatoid arthritis, RA)是以滑膜组织为靶点的慢性系统性自身免疫性疾病。
- 人群负担显著(全球约 1%;美国成人估计约 1.3 million),且 RA 仍是工作失能的重要原因。
- 典型表现为双侧、对称性炎性关节痛、肿胀及晨僵时间延长。
- RA 常呈缓解-加重交替模式,并有间歇性症状发作。
- 妊娠期部分患者症状可改善,但剖宫产、子痫前期与早产风险仍可能升高。
- 若未早期治疗,疾病进展可导致畸形、挛缩与功能下降。
- 核心治疗将症状控制与疾病修饰治疗结合,以减缓关节损伤。
- 护理优先项聚焦疼痛控制、活动能力保留、皮肤/关节保护及感染风险教育。
病理生理
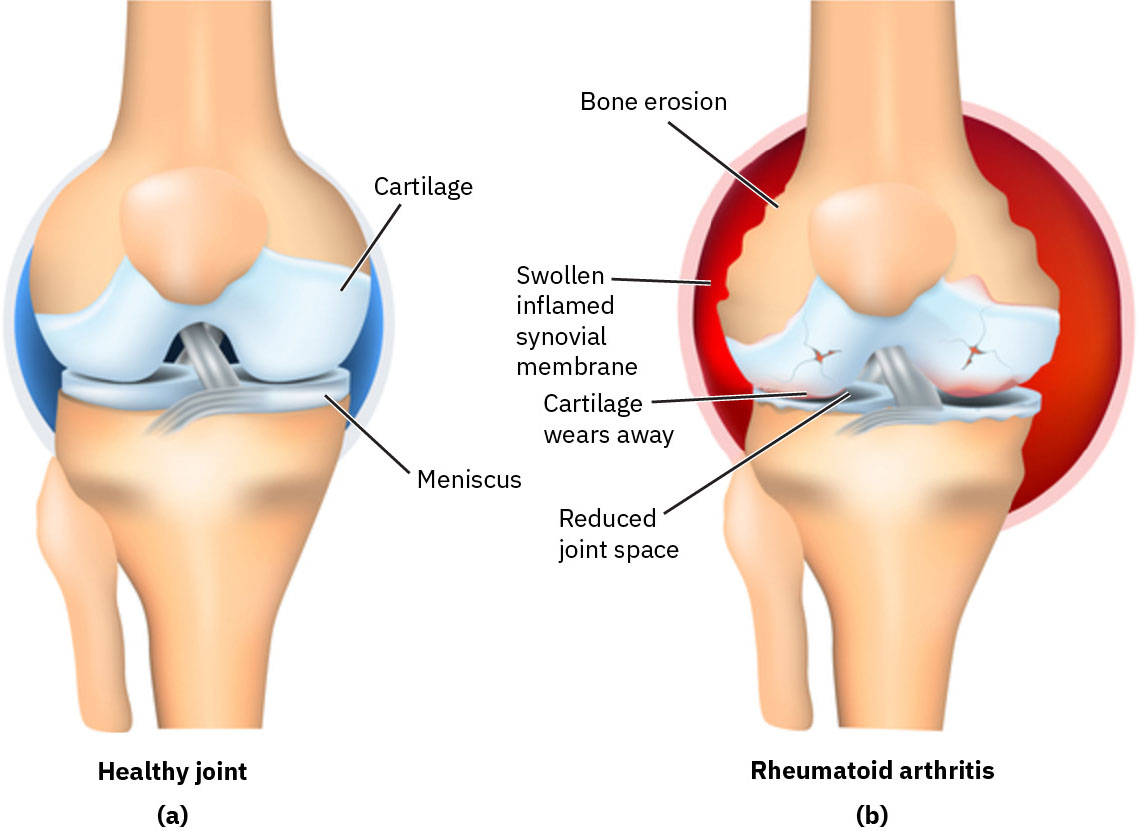 Illustration reference: OpenStax Clinical Nursing Skills Ch.25.
Illustration reference: OpenStax Clinical Nursing Skills Ch.25.
RA 是一种免疫介导炎症性疾病,机体会攻击滑膜。持续性滑膜炎会损伤软骨、骨及邻近结构,导致慢性疼痛和进行性关节功能障碍。 在遗传易感个体中,吸烟或石棉暴露等环境触发因素可促成自身抗体激活与炎性关节破坏。
炎症过程通常为双侧并累及多个关节,尤以手部和腕部常见。随时间推移,未治疗炎症可导致关节不稳定、关节活动范围下降、失用性肌萎缩及特征性畸形。
分类
- 早期 RA:关节压痛、温热、肿胀、疲劳及晨僵持续超过 30 分钟。
- 晚期 RA:重度畸形(包括天鹅颈或钮扣花样畸形)、挛缩、不稳定及明显功能丧失。
- RA 全身受累:关节外效应可包括胸膜炎样症状、神经病理发现及炎症性眼部并发症。
风险因素
- 女性,以及发病常见于成年早中期。
- 在许多队列中,女性患病率约为男性的两倍。
- 家族史与遗传易感性。
- 可放大免疫失调的慢性压力负担。
- 环境暴露(例如吸烟和石棉暴露)可在遗传易感个体中增加风险。
护理评估
NCLEX 重点
优先识别炎症性与退行性关节模式差异,并监测限制功能的进展。
- 评估双侧关节疼痛、肿胀、红斑、温热及晨僵时间延长。
- 评估类风湿结节,尤其是受压区域与伸侧表面。
- 评估双侧握力与手部功能使用,因为手关节受累常见且常致残。
- 在以手部为主的表现中,评估双侧 MCP/PIP 压痛、水肿、红斑及疼痛限制的手指 ROM。
- 区分 RA 与骨关节炎模式:RA 通常为炎症性且对称,而 OA 更偏磨损相关,且疾病早期常较不对称。
- 评估功能与活动能力,包括关节活动范围、步态受限、疲劳负担及 ADL 影响。
- 评估全身性发作线索(例如低热、不适、食欲减退和异常疲劳),这些线索可先于或伴随炎症性关节恶化出现。
- 监测畸形进展(包括天鹅颈与钮扣花样改变)及挛缩形成。
- 复核支持炎症性自身免疫疾病的诊断趋势,包括 RF、ANA、ESR 和 CRP。
- 触诊时若出现“海绵样”关节质地需记录,因为这支持活动性炎性滑膜炎。
- 识别 RF 在相当比例 RA 病例中阳性(队列中约 90%),但解释应结合临床与炎症指标背景。
- 使用影像学(X 线、超声、MRI)评估侵蚀性损伤,同时认识到早期 RA 可出现影像正常,不应仅凭影像排除。
- 在有妊娠可能患者中,评估当前 RA 用药安全,并强化早期报告疲劳、关节痛或肿胀加重。
- 当使用免疫抑制剂或生物制剂治疗时,评估关节外表现及感染风险。
分期模式发现
- 早期 RA:
- 对称性多关节疼痛/压痛,伴温热和红斑。
- 晨僵持续超过 30 分钟。
- 疲劳与肌无力。
- 可能出现轻度胸膜炎样症状、心包摩擦音、神经病理性感觉异常或眼干/刺激感。
- 晚期 RA:
- 进展性畸形、挛缩、不稳定、ROM 明显受限及失用性肌萎缩。
- 心血管风险升高(动脉粥样硬化负担加速)。
- 胸膜炎/间质性肺病进展风险。
- 周围神经病变及炎症性眼受累(例如巩膜炎)。
护理干预
- 采用结构化疼痛复评,并结合药物与非药物策略,如热敷、冷敷、放松和活动节律化。
- 强化关节保护技术、夹板或支具正确使用,以及受压高风险部位常规皮肤检查。
- 支持物理治疗与作业治疗计划,以保留柔韧性、肌力和独立功能。
- 按医嘱协调结合 DMARD、NSAID 和糖皮质激素路径的用药计划,并在计划减停激素时强化依从递减方案。
- 强化休息与活动交替安排,以减少炎性关节应力且避免完全去条件化。
- 教授节能方法与家庭/工作情境中的适配设备使用。
- 在妊娠计划或妊娠期,按指征协调用药复核咨询与高危产科转介。
- 对免疫抑制治疗提供感染预防教育,包括卫生习惯、疫苗更新、暴露回避与早期症状报告。
- 监测并保护结节部位或支具/夹板受压点皮肤完整性。
免疫抑制下的感染预防教育
- 强化持续执行 手卫生 与个人卫生习惯。
- 避免与有症状患者近距离接触。
- 与照护团队协作维持推荐疫苗接种。
- 采用安全食物处理流程以降低食源性感染风险。
- 在可能时减少在拥挤暴发环境中的暴露。
- 在医疗环境或高风险公共场所按指征使用防护装备。
- 保持家庭环境卫生并常规进行表面消毒。
- 及时报告感染症状,并与医师保持主动沟通。
倡导与心理社会支持
- 协调多学科 RA 照护(护理、风湿科、PT、OT 及其他所需专科)。
- 处理治疗可及性障碍并支持自我管理规划。
- 强化关节保护、节能与以独立性为目标的辅助器具使用。
- 使用 治疗性沟通 处理慢病痛苦,并鼓励参与支持小组/社区资源。
常见护理诊断
- 慢性疼痛。
- 活动受限。
- 疲劳。
- 皮肤完整性受损风险。
结局指标
- 在计划时限内将疼痛降至个体化目标(例如 ≤ 3/10)。
- 正确执行处方运动与活动支持技术。
- 疲劳负担下降且 ADL 参与改善。
- 高风险受压/结节区域皮肤完整。
- 随访评估显示 ROM 改善、肿胀/僵硬负担下降及握力增强。
- 治疗监测期间未报告明显药物不良反应。
高风险免疫抑制治疗效应
DMARD 与生物制剂可导致严重不良反应和感染易感性升高,需密切监测并对可疑发现快速升级处理。
药理学
| 药物类别 | 示例 | 关键护理注意事项 |
|---|---|---|
| [nsaids] | 布洛芬(ibuprofen)、萘普生(naproxen) | 改善疼痛与炎症;监测疗效与耐受性。 |
| [analgesics] | acetaminophen、选择性阿片类使用 | 症状控制辅助方案;复评获益-风险与功能结局。 |
| [corticosteroids] | prednisone、关节腔内糖皮质激素 | 短期发作控制;监测不良反应(例如体重增加、骨质疏松、感染风险),并谨慎减量以降低肾上腺功能不全风险。 |
| [disease-modifying-antirheumatic-drugs] (抗疟药) | 羟氯喹(hydroxychloroquine)、氯喹(chloroquine) | 在部分方案中用于控制炎症症状并减少发作。 |
| [immunosuppressants] | 环磷酰胺(cyclophosphamide,重症情境) | 仅用于高严重度疾病;密切监测毒性与感染风险。 |
| [disease-modifying-antirheumatic-drugs] | 甲氨蝶呤(methotrexate)、柳氮磺吡啶(sulfasalazine) | 减缓疾病进展;甲氨蝶呤在妊娠期禁用,且需进行孕前用药复核。 |
| [biologic-response-modifiers] | 类别性生物制剂 | 靶向免疫通路;密切监测感染风险。 |
| [biologic-response-modifiers] (肿瘤坏死因子抑制剂) | 英夫利昔单抗(infliximab)、阿达木单抗(adalimumab) | 降低炎症活性;在存在活动性感染或严重感染风险时谨慎使用。 |
临床判断应用
临床情景
一名中年来访者报告双侧手痛、晨僵时间延长、疲劳,并在穿衣和备餐方面困难加重,同时炎症指标升高。
- 识别线索:对称性炎症性关节发现并伴功能下降。
- 分析线索:该模式支持活动性自身免疫性滑膜炎并存在进展风险。
- 确定优先假设:最高优先项是在保留独立性与安全的同时限制关节损伤。
- 提出解决方案:优化疼痛控制、强化治疗参与并加强自我管理教育。
- 采取行动:实施活动与皮肤/关节保护计划,监测用药效应并升级恶化发现。
- 评估结局:疼痛下降、日常功能改善,且未见新发畸形进展。
评价
- 在既定时间目标内复评结局为达成、部分达成或未达成。
- 当症状控制、活动能力、疲劳或皮肤目标未达成时修订照护计划。
- 在干预后、诊断/化验更新后及跨专业照护计划复核后再次评估。
相关概念
- 常见肌肉骨骼疾病识别与照护优先事项 - 慢性关节疾病间的鉴别模式识别。
- 跌倒预防 - 活动下降与无力会增加跌倒和损伤风险。
- 肾脏疾病 - 慢病管理中的共病与用药安全情境。
- 日常生活活动 - RA 症状负担常降低独立自我照护能力。
- 创伤知情照护 - 慢性疼痛与残障需要支持性、以人为中心的沟通策略。
自我检查
- 哪些发现最能区分早期炎症性 RA 与晚期结构性 RA 损伤?
- 即使短期镇痛可改善症状,为什么仍优先使用 DMARD?
- 在生物制剂或其他免疫抑制治疗期间,哪些教育要点最能降低感染风险?