慢性阻塞性肺疾病 (Chronic Obstructive Pulmonary Disease)
要點
- COPD 是由慢性支氣管炎、肺氣腫或兩者共同導致的進行性發炎性氣流受限。
- COPD 疾病負擔仍高,對美國住院率與死亡率有顯著影響。
- 慢性低氧血症與高碳酸血症會驅動症狀負擔與急性惡化風險。
- 急性惡化是 COPD 相關住院與死亡加速的主要原因。
- 在 COPD 中,低 BMI 與進行性肌肉流失是預後不良線索,與橫膈肌無力、肺功能下降與死亡風險上升相關。
- 透過少量多餐、維持直立姿勢與節能節奏,可減少進食相關呼吸困難。
- 在合併低氧血症的 COPD 中,富含抗氧化成分且含 lycopene 食物的飲食型態,可能支持肺部營養目標。
- 進行性食慾不振與營養不良會削弱咳嗽效能、增加分泌物滯留,並提高肺炎風險負擔。
- 護理重點聚焦於氧合監測、支氣管擴張劑治療與自我管理教育。
病理生理
COPD 由長期暴露於刺激物(主要為香菸煙霧)所致,造成氣道發炎、黏液過度分泌(慢性支氣管炎),以及肺泡破壞與彈性回縮喪失(肺氣腫)。氣流受限多為不可逆且具進行性。
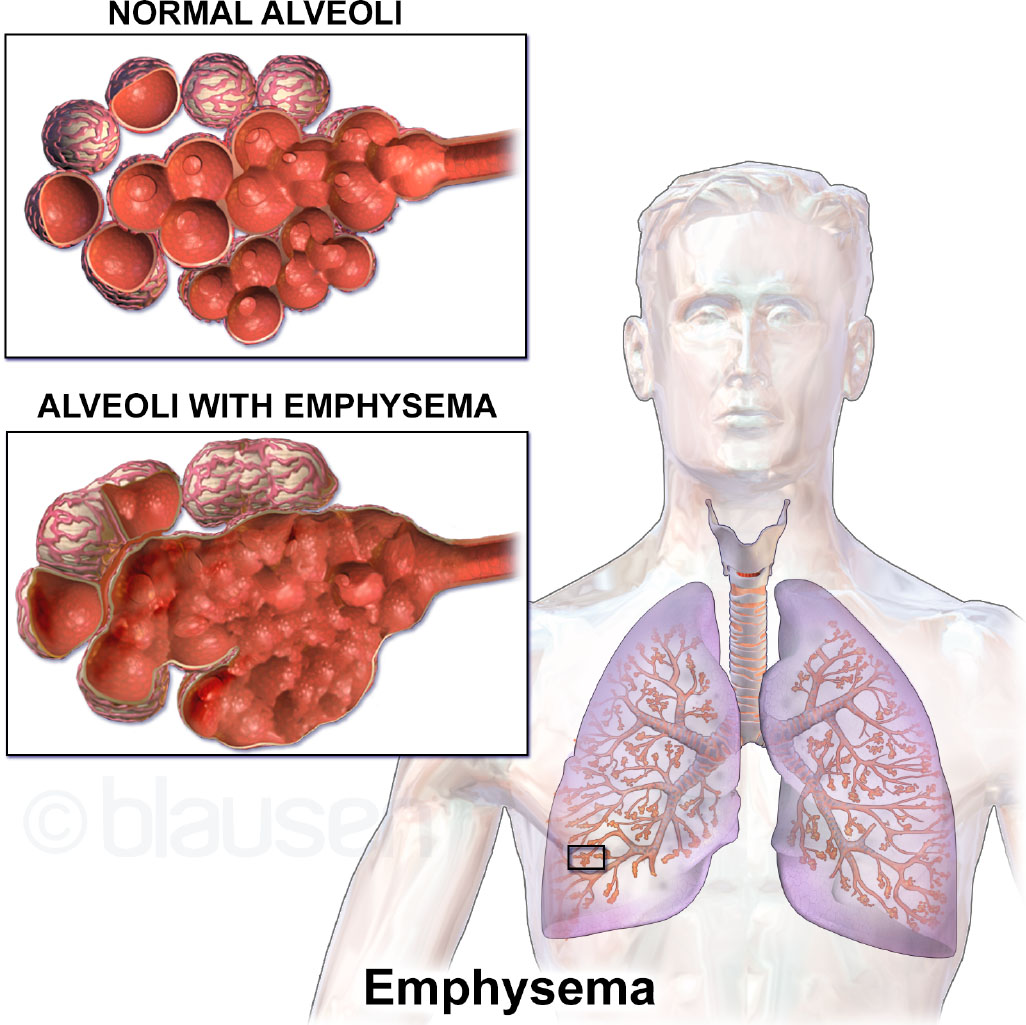 Illustration reference: OpenStax Medical-Surgical Nursing Ch.11.5.
Illustration reference: OpenStax Medical-Surgical Nursing Ch.11.5.
發炎性損傷可影響氣道、肺血管與肺組織;常見重塑變化包含氣道狹窄、平滑肌肥厚,以及最終形成與疤痕相關的固定性狹窄。 當肺泡壁失去彈性時,呼氣效率下降且二氧化碳滯留惡化。 COPD 可治療但無法治癒;症狀通常在肺損傷顯著後才會明顯,且若持續暴露於煙霧,常會隨時間惡化。
在部分個案中,alpha-1 antitrypsin 缺乏會因降低對蛋白酶介導組織損傷的保護,而促成肺氣腫性肺損傷。 與吸菸相關分布型態相比,alpha-1 antitrypsin 缺乏相關 COPD 可呈現以下葉為主的肺氣腫侵犯。
慢性低氧血症會刺激紅血球生成(次發性紅血球增多症)與肺血管收縮(重症時可見肺心病)。當呼吸肌疲勞限制代償時,便會發展為高碳酸血症。 COPD 亦與共病負擔增加相關,包含心血管疾病與 肺癌。 美國中高齡成人 COPD 盛行率仍高,且年度死亡負擔顯著。
分類
- 慢性支氣管炎:連續 2 年中每年咳痰至少 3 個月;屬於「blue bloater」型態。
- 肺氣腫:肺泡破壞與空氣滯留;屬於「pink puffer」型態並常見桶狀胸。
- GOLD 分類:依 FEV₁ % predicted 分級(I: >=80,II: 50-79,III: 30-49,IV: <30),並整合症狀/急性惡化負擔。
- 風險因子輪廓:可改變風險包含吸菸、二手菸、職業粉塵/煙霧暴露與室內生物質煙霧。不可改變風險包含年齡大於 40 歲、兒童期呼吸道感染、氣喘病史、早產相關肺發育不足與 alpha-1 antitrypsin 缺乏。
- 吸菸暴露型態:COPD 常與約 10-15 pack-years 以上的吸菸暴露相關;環境/職業暴露亦可解釋相當比例的非吸菸者亞群。
- 族群負擔輪廓:盛行率與死亡率受結構性因素與暴露負擔影響,對部分種族化社群造成不成比例影響。
護理評估
NCLEX 重點
在 COPD 中需謹慎監測 O₂ 飽和度,重症時高流量氧氣可能抑制低氧驅動。
- 於基線與急性惡化期間評估呼吸困難、咳嗽、痰液產生與活動耐受度。
- 辨識成人發病的進展型態,以及許多個案在寒冷季節症狀加劇的趨勢。
- 聽診是否有呼氣延長、喘鳴與呼吸音減弱。
- 監測氧飽和度,對高碳酸血症型 COPD 的目標為 88–92%,以保留低氧驅動。
- 趨勢追蹤靜息與活動時氧飽和度,並與既有基線比較,因早期勞力性去飽和可先於嚴重功能退化出現。
- 監測晚期疾病常見的反覆呼吸道感染、進行性疲倦、桶狀胸、發紺與非預期體重下降。
- 監測惡病質與杵狀指作為晚期慢性疾病線索。
- 將低 BMI 合併肌肉量下降視為高風險營養發現,因其與較低運動耐受與較差 COPD 結局相關。
- 不可僅依賴 BMI:部分體重較高個案仍可能有去脂體重偏低與具臨床意義的肺部營養不良風險。
- 評估肺心病徵象:周邊水腫、JVD、肝腫大。
- 評估暴露史(職業性微粒、室內煤/木材煙霧、二手菸)與不可改變 COPD 風險線索(兒童期感染、早產、alpha-1 antitrypsin 缺乏病史)。
- 篩檢焦慮與憂鬱,這些常見共病會影響治療遵從性。
- 以肺量計標準進行診斷/分期:FEV₁/FVC 低於約 0.70 支持 COPD,再以 GOLD FEV₁ 範圍分期嚴重度。
- 疑似急性惡化時,追蹤核心三聯徵(呼吸困難增加、痰量增加、痰液膿性增加),並搭配發燒、近期 URI 與相對基線的心搏過速/呼吸過速等附加徵象。
- 存在氧合疑慮時,結合 pulse oximetry 與 ABG 評估;PaCO2 高於約 45 mmHg 且合併酸血症,支持高碳酸性呼吸性酸中毒風險。
護理介入
- 依醫囑給予支氣管擴張劑(短效 beta-agonists、anticholinergics)與皮質類固醇。
- 採高 Fowler’s 或 tripod 姿勢以最大化呼吸作功。
- 教導縮唇呼吸與橫膈呼吸,以減少空氣滯留。
- 區分控制藥與急救吸入器:每日使用 吸入型皮質類固醇(例如 fluticasone)並於用藥後漱口;使用 albuterol 以快速緩解呼吸困難。
- 進行戒菸衛教,這是目前唯一被證實可減緩疾病進展的介入。
- 提供家庭去菸暴露諮詢,包含二手菸危害(非吸菸者肺癌風險增加,且兒童下呼吸道感染、SIDS、耳部感染與氣喘惡化風險上升)。
- 分段安排 ADLs 並採取有利呼吸的姿勢,以減少日常活動中的呼吸困難負擔。
- 強化已開立補充氧氣的治療遵從性。
- 協調符合條件個案轉介肺部復健。
- 規劃 日常生活活動 的節能策略。
- 對重度呼吸困難且有營養不良/惡病質風險者,於臨床適當時協調高熱量攝取的營養支持規劃。
- 當攝取下降時,監測咳嗽無力/分泌物清除不佳並及早升級處置,以降低肺炎風險進展。
- 針對進食相關呼吸困難或疲勞,教導每日 4-6 次少量進食、進食時維持直立、放慢每口速度並配合呼吸停頓,以及在飽脹加重呼吸作功時把液體安排於兩餐之間。
- 在合併低氧血症的 COPD 中,強化抗氧化導向飲食選擇(例如水果、蔬菜、全穀、堅果與富含 lycopene 食物),並納入個案熱量與體重目標。
- 若腹脹加重呼吸作功,個別化低產氣飲食規劃並重評耐受度。
- 於急性惡化期間與之後,趨勢追蹤體重與攝取量,因反覆急性惡化可加速體重與肌肉流失。
- 在具高碳酸風險的急性惡化中啟動氧療後,於約 30-60 分鐘內重評 CO2 滯留惡化線索,並依需要升級處置。
- 協調跨專業出院規劃(呼吸治療、藥學、營養、社會支持與復健)以降低再住院風險。
氧氣給藥
在慢性高碳酸血症型 COPD 中,過量氧氣(>92%)可能抑制低氧呼吸驅動。應謹慎滴定 O₂,目標為 88–92%。
藥理學
| 藥物類別 | 範例 | 重要考量 |
|---|---|---|
| 短效支氣管擴張劑 | Albuterol (SABA)、ipratropium (SAMA) | 急救使用;教導吸入器技巧 |
| 長效支氣管擴張劑 | Salmeterol (LABA)、tiotropium (LAMA) | 維持治療;不適用於急性緩解 |
| [corticosteroids] | Prednisone、budesonide/formoterol | 急性惡化:口服全身性;維持治療:吸入型 |
| 磷酸二酯酶-4 抑制劑 | Roflumilast | 適用於合併慢性支氣管炎的重度 COPD |
臨床判斷應用
臨床情境
一名 COPD 個案使用 2L 鼻導管時發生呼吸困難惡化。SpO₂ 為 86%。護理師將 O₂ 提高至 6L。
- 辨識線索:O₂ 飽和度偏低,但快速提高高流量有抑制低氧驅動風險。
- 分析線索:個案有慢性高碳酸血症;目標應為 88–92%,而非常氧。
- 優先排序假設:高碳酸個案因過量 O₂ 導致呼吸抑制的風險。
- 提出解決方案:將 O₂ 滴定至 88–92%,頻繁重評,並在需要時準備升級。
- 採取行動:調整至可達目標 SpO₂ 的最低 O₂ 流量;通知醫療提供者;監測 ABGs。
- 評估結果:SpO₂ 維持於安全範圍,且無呼吸抑制惡化。
相關概念
- 氣喘行動計畫與急性惡化管理 - 阻塞型肺病比較與鑑別。
- 呼吸系統 - 正常氣道生理與防禦機制。
- 氧氣治療 - 氧氣輸送系統 與呼吸疾病中的監測。
- 實證呼吸照護 - COPD 中的支氣管衛生與氣道清除技術。
自我檢核
- 為何高流量氧氣對高碳酸型 COPD 個案可能危險?
- 臨床上慢性支氣管炎與肺氣腫有何區別?
- 哪項介入對減緩 COPD 進展的證據最強?