慢性阻塞性肺疾病 (Chronic Obstructive Pulmonary Disease)
关键要点
- COPD 是由慢性支气管炎、肺气肿或两者共同导致的进行性炎性气流受限。
- COPD 负担仍然很高,在美国对住院率和死亡率具有显著影响。
- 慢性低氧血症和高碳酸血症驱动症状负担及急性加重风险。
- 急性加重是 COPD 相关住院和死亡加速的主要原因。
- 在 COPD 中,低 BMI 和进行性肌肉流失是预后不良线索,与膈肌无力、肺功能下降和死亡风险增加相关。
- 通过少量多餐、保持直立体位和节能节律可减轻进食相关呼吸困难。
- 在合并低氧血症的 COPD 中,富含抗氧化剂(包括富含 lycopene 的食物)的饮食模式可支持肺部营养目标。
- 进行性厌食和营养不良可削弱咳嗽效果、增加分泌物潴留并提高肺炎风险负担。
- 护理重点聚焦于氧合监测、支气管扩张剂治疗和自我管理教育。
病理生理学
COPD 由长期暴露于刺激物(主要是香烟烟雾)引起,导致气道炎症、黏液高分泌(慢性支气管炎)及肺泡破坏并失去弹性回缩(肺气肿)。气流受限大多不可逆且呈进行性。
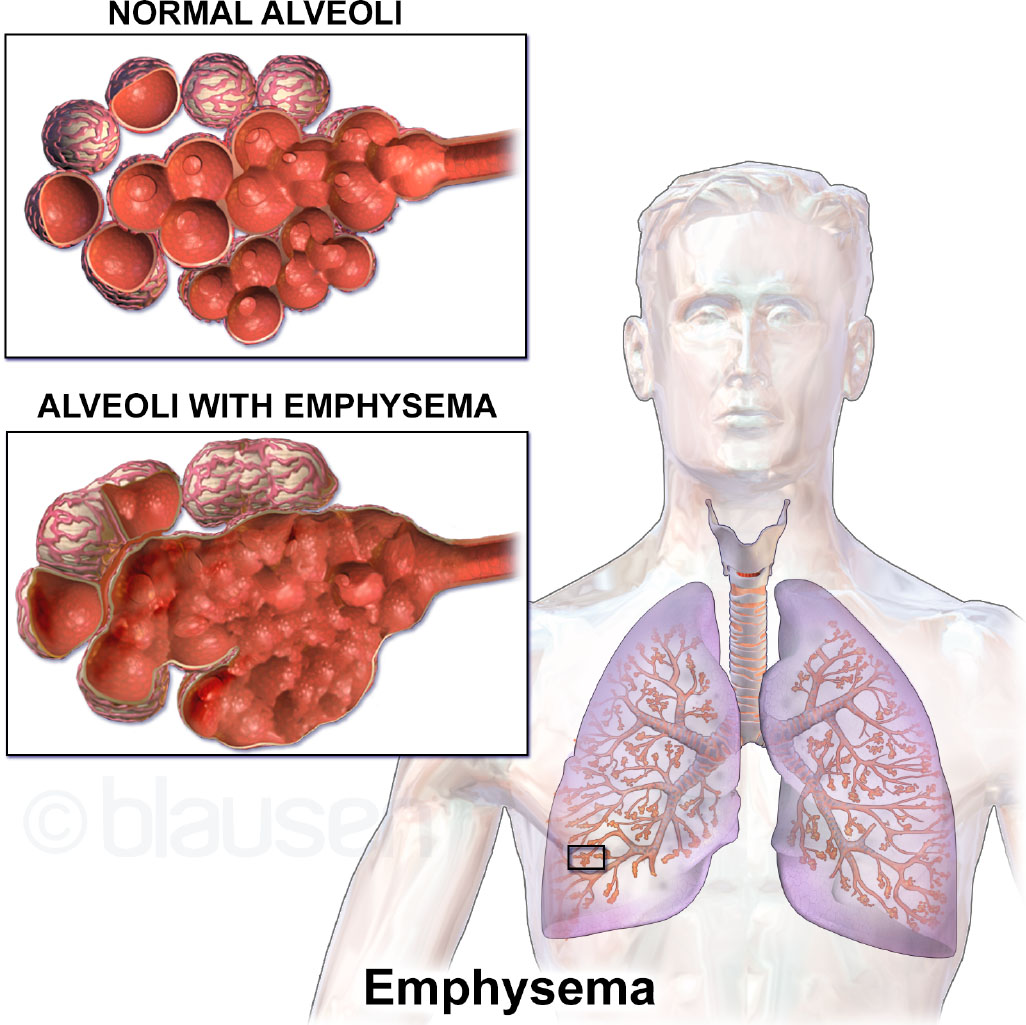 Illustration reference: OpenStax Medical-Surgical Nursing Ch.11.5.
Illustration reference: OpenStax Medical-Surgical Nursing Ch.11.5.
炎症性损伤可累及气道、肺血管和肺组织;常见重塑变化包括气道狭窄、平滑肌肥厚,以及最终的瘢痕相关固定性狭窄。 当肺泡壁失去弹性时,呼气效率下降且二氧化碳潴留加重。 COPD 可治疗但不可治愈;症状通常在肺损伤已较明显后才出现,且在持续烟雾暴露时往往随时间加重。
在部分患者中,α1 抗胰蛋白酶缺乏会因减少对蛋白酶介导组织损伤的保护而促成肺气肿性肺损伤。 与吸烟相关分布模式相比,α1 抗胰蛋白酶缺乏相关 COPD 可表现为下叶优势型肺气肿受累。
慢性低氧血症可刺激红细胞生成(继发性红细胞增多)及肺血管收缩(重症时出现肺心病)。当呼吸肌疲劳限制代偿时,会发展为高碳酸血症。 COPD 还与共病负担增加相关,包括心血管疾病和 肺癌。 美国中老年人群 COPD 患病率仍较高,年度死亡负担显著。
分类
- 慢性支气管炎: 连续 2 年中每年咳痰 ≥3 个月;“蓝肿型(blue bloater)”模式。
- 肺气肿: 肺泡破坏与气体潴留;“粉喘型(pink puffer)”模式并可见桶状胸。
- 慢阻肺分级体系(GOLD): 按 FEV₁ % predicted 分级(I: ≥80,II: 50-79,III: 30-49,IV: <30),并整合症状/急性加重负担。
- 风险因素特征: 可改变风险包括吸烟、二手烟、职业粉尘/烟雾暴露和室内生物质烟雾。不可改变风险包括年龄 >40 岁、儿童期呼吸道感染、哮喘史、早产相关肺发育不足及 α1 抗胰蛋白酶缺乏。
- 吸烟暴露模式: COPD 常与约 10-15 pack-years 以上吸烟暴露相关;环境/职业暴露也可解释相当比例非吸烟者亚群。
- 人群负担特征: 患病率和死亡率受结构性因素及暴露负担影响,对部分种族化社区影响不成比例。
护理评估
NCLEX 重点
在 COPD 中需谨慎监测 O₂ 饱和度——重症时高流量氧可抑制低氧驱动。
- 在基线及急性加重期间评估呼吸困难、咳嗽、痰液产生和活动耐受性。
- 识别成人期起病进展模式及许多患者在寒冷季节症状加重的特点。
- 听诊是否存在呼气延长、喘鸣和呼吸音减弱。
- 监测氧饱和度——对高碳酸血症型 COPD 目标为 88-92%,以维持低氧驱动。
- 追踪静息与活动后氧饱和度并与既往基线比较,因为早期劳力性去饱和可先于严重功能下降。
- 在晚期疾病中监测反复呼吸道感染、进行性疲劳、桶状胸、发绀及非意愿体重下降。
- 监测恶病质和杵状指作为晚期慢性病线索。
- 将低 BMI 合并肌肉量下降视为高风险营养发现,因为其与更低运动耐受和更差 COPD 结局相关。
- 不要仅依赖 BMI:部分体重较高患者仍可能存在去脂体重低和具有临床意义的肺部营养不良风险。
- 评估肺心病体征:外周水肿、JVD、肝大。
- 评估暴露史(职业颗粒物、室内煤/木烟、二手烟)及不可改变 COPD 风险线索(儿童期感染、早产、α1 抗胰蛋白酶缺乏史)。
- 筛查焦虑和抑郁,这些常见共病会影响依从性。
- 使用肺功能标准进行诊断/分期:FEV₁/FVC 低于约 0.70 支持 COPD,再用 GOLD FEV₁ 范围分级严重度。
- 当怀疑急性加重时,追踪核心三联征(呼吸困难增加、痰量增加、痰脓性增加)以及发热、近期 URI 和相对基线的心动过速/呼吸增快等附加体征。
- 当存在氧合问题时联合使用脉搏血氧与 ABG;PaCO2 高于约 45 mmHg 且伴酸血症,提示高碳酸性呼吸性酸中毒风险。
护理干预
- 按医嘱给予支气管扩张剂(短效 β2 激动剂、抗胆碱药)和皮质类固醇。
- 采用高 Fowler 位或 tripod 位以最大化呼吸做功。
- 教授缩唇呼吸和膈肌呼吸以减少气体潴留。
- 区分控制药与急救吸入器:每日使用 吸入性皮质类固醇(例如 fluticasone)并在用后漱口;使用 沙丁胺醇(albuterol) 快速缓解呼吸困难。
- 开展戒烟教育——这是目前唯一被证实可减缓疾病进展的干预。
- 教授家庭去烟咨询,包括二手烟危害(非吸烟者肺癌风险增加,以及儿童下呼吸道感染、SIDS、耳部感染和哮喘加重风险升高)。
- 分段安排 ADLs 并采取有利呼吸体位,以减少日常活动中的呼吸困难负担。
- 强化医嘱补充氧依从性。
- 为符合条件患者协调肺康复转诊。
- 规划 日常生活活动 的节能策略。
- 对重度呼吸困难且有营养不良/恶病质风险者,在临床适宜时协调高热量摄入营养支持计划。
- 当摄入下降时,监测咳嗽无力/分泌物清除不良并尽早升级处置,以降低肺炎风险进展。
- 对进食相关呼吸困难或疲劳,教授每日 4-6 次少量进食、进食时保持直立、放慢每口速度并配合呼吸停顿,以及当饱胀加重呼吸负担时将液体安排在两餐间。
- 在合并低氧血症的 COPD 中,强化抗氧化导向选择(例如水果、蔬菜、全谷物、坚果及富含 lycopene 的食物),并结合患者热量和体重目标。
- 若腹胀加重呼吸负担,个体化低产气饮食计划并复评耐受性。
- 在急性加重期间及之后追踪体重与摄入,因为反复急性加重可加速体重和肌肉流失。
- 在高碳酸风险急性加重中启动氧疗后,于约 30-60 分钟内复评 CO2 潴留恶化线索,并按需升级处置。
- 协调跨学科出院计划(呼吸治疗、药学、营养、社会支持与康复)以降低再入院风险。
氧疗给药
在慢性高碳酸型 COPD 中,过量氧疗(>92%)可抑制低氧性呼吸驱动。应谨慎滴定 O₂,目标 88-92%。
药物治疗
| 药物类别 | 示例 | 关键注意事项 |
|---|---|---|
| 短效支气管扩张剂 | Albuterol(SABA)、ipratropium(SAMA) | 用于急救;教授正确吸入器技术 |
| 长效支气管扩张剂 | Salmeterol(LABA)、tiotropium(LAMA) | 维持治疗;不用于急性缓解 |
| [corticosteroids] | Prednisone、budesonide/formoterol | 急性加重:口服全身用药;维持:吸入治疗 |
| 磷酸二酯酶-4 抑制剂 | Roflumilast | 适用于伴慢性支气管炎的重度 COPD |
临床判断应用
临床情景
一名 COPD 患者使用 2L 鼻导管时出现呼吸困难加重。SpO₂ 为 86%。护士将 O₂ 提高至 6L。
- 识别线索: O₂ 饱和度偏低,但快速提高高流量氧有抑制低氧驱动风险。
- 分析线索: 患者存在慢性高碳酸血症;目标应为 88-92%,而非追求常氧。
- 确定优先假设: 高碳酸患者因过量 O₂ 发生呼吸抑制的风险。
- 提出解决方案: 将 O₂ 滴定至 88-92%,频繁复评,并在需要时准备升级。
- 采取行动: 调整至达到目标 SpO₂ 的最低 O₂ 流量;通知医师;监测 ABGs。
- 评估结局: SpO₂ 维持在安全范围,且无呼吸抑制加重。
相关概念
- 哮喘行动计划与急性加重管理 - 阻塞性肺病比较与鉴别。
- 呼吸系统 - 正常气道生理与防御机制。
- 氧疗 - 氧输送系统 及呼吸系统疾病中的监测。
- 循证呼吸护理 - COPD 中的支气管卫生与气道清除技术。
自我检测
- 为什么高流量氧疗对高碳酸型 COPD 患者可能危险?
- 临床上如何区分慢性支气管炎与肺气肿?
- 哪项干预对减缓 COPD 进展的证据最强?