單位劑量腸道外給藥配製(小瓶、安瓿與復溶)
重點整理
- 腸道外給藥可繞過胃腸道吸收與首渡代謝,在不適合口服時提供更快且更可預測的全身效應。
- 安全配製需要嚴格無菌、正確稀釋液選擇,以及準確劑量/體積計算。
- 單劑量小瓶使用一次即丟棄;安瓿抽取需使用濾針技術。
- 安瓿抽藥時,不可向安瓿注入空氣,也不可將已抽入的氣泡再排回安瓿。
- 復溶必須遵循廠商說明,包含稀釋液類型、體積、濃度與保存條件。
- 復溶說明必須始終由權威標示/eMAR 資源核實,不可憑經驗假設。
- 復溶換算應以標示之復溶後濃度進行給藥劑量計算;除非標示明確指示,否則不可用乾粉瓶標示量、僅稀釋液體積或估算置換體積替代。
- 同一注射器混藥前,必須先確認相容性並遵守途徑特異體積上限。
- 多劑量小瓶處理需標註開封日期與超過可用日期(beyond-use date, BUD;常見最長 28 天,除非廠商標示要求更早丟棄)。
- 針頭選擇必須符合途徑/部位/體型與醫囑體積;針規數字越大代表針徑越小。
- 注射器選擇應同時符合目標體積與刻度精度(例如較小容量注射器提供較細刻度)。
- 各途徑常見選擇包含 ID/SQ 較細針規,以及多數 IM 配製較低針規,並對極瘦/惡病質病人進行個別化調整。
- 預充式卡匣/注射裝置在核實產品完整性與給藥途徑指示後,可提升速度、劑量準確度與污染控制。
- 預充注射器的空氣管理需依產品特定規則;部分產品(例如 enoxaparin 預充注射器)需保留廠商預留氣泡。
- 危害性/細胞毒性藥物復溶需符合防護控制、PPE 與藥局受訓流程。
- 混合後總體積必須維持在途徑/部位與年齡特異耐受上限內,以避免疼痛、吸收不良與局部不良事件。
設備
- MAR 與有效開立醫囑查閱
- 醫囑藥物容器(單劑量小瓶、多劑量小瓶、安瓿或預充卡匣)
- 無菌注射器/針頭選項(包含 Luer-lock 或 Luer-slip 連接,以及胰島素/結核菌素注射器等固定針型)加上安瓿抽取用濾針
- 條件可行時使用無針/鈍針小瓶取藥裝置以降低銳器風險
- 核准稀釋液與廠商/包裝說明
- 酒精棉片、手套、銳器盒與標示/紀錄工具
步驟流程
- 核對病人、醫囑、給藥途徑適配性(例如口服不耐受或需非口服起效)、用藥權核對、濃度、效期與途徑特異體積上限。
- 執行 手部衛生,準備乾淨且低干擾的作業區。
- 設置全程維持注射裝置無菌:未使用時針頭保持帶帽,避免污染注射器活塞桿/Luer 連接表面。
 Illustration reference: OpenStax Clinical Nursing Skills Ch.12.
Illustration reference: OpenStax Clinical Nursing Skills Ch.12. - 依溶液特性與目標體積選擇適當注射器與針頭規格/連接型式(常見注射器容量約 0.5-60 mL;多數成人 IV 推注劑量常配製於 3、5 或 10 mL 注射器)。針規/針長選擇應反映注射部位、病人體型/身體組成與劑量體積;需安全旋鎖連接時使用 Luer-lock,在裝置情境適合快速接裝/拆卸時可使用 Luer-slip/slip-tip。打開無菌包裝後,以筒身持握注射器並保持注射器尖端/活塞無菌。判讀注射器體積時,以活塞與液體接觸之前緣為準,並使注射器容量符合所需量測精度(例如 1 mL 常見百分位刻度、3 mL 常見十分位刻度、多數 5-12 mL 常見五分位/五分之二刻度、大型 60 mL 注射器常見整數刻度)。
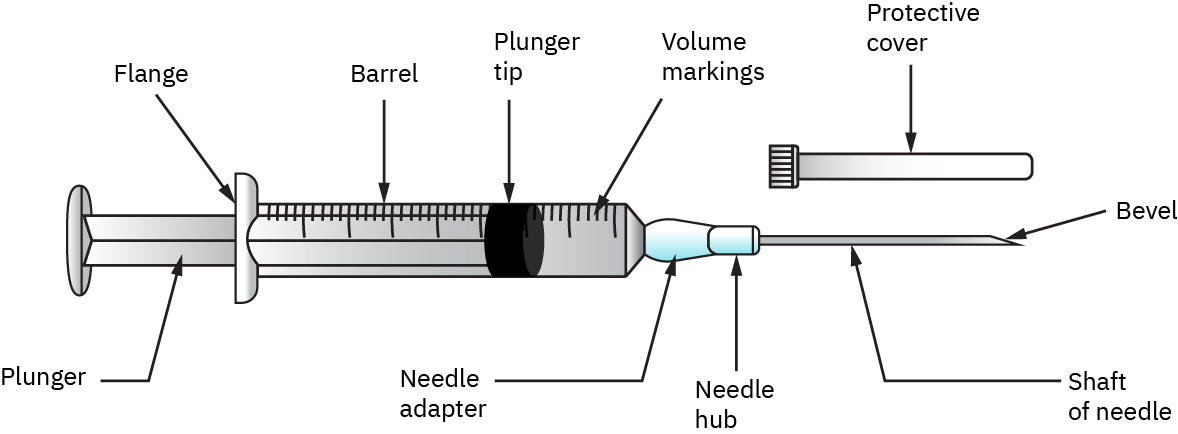 Illustration reference: OpenStax Clinical Nursing Skills Ch.12.
Illustration reference: OpenStax Clinical Nursing Skills Ch.12.
 Illustration reference: OpenStax Pharmacology Ch.2.3.
Illustration reference: OpenStax Pharmacology Ch.2.3. - 針對小瓶,移除防塵蓋(非無菌)、以 70% isopropyl alcohol 擦拭橡皮隔膜、依指示注入空氣(常為與預計抽取體積相同)、抽藥時針尖保持在藥液中,並以無菌技術抽取精確體積。
- 若使用多個小瓶,每個小瓶需使用獨立酒精棉片,並維持獨立無菌取藥事件。
- 針對多劑量小瓶,依政策/廠商指引標示開封日期與超過可用日期(常見最長 28 天,除非廠商標示要求更早丟棄)。
- 除非政策要求以受控方式在床邊使用,否則多劑量小瓶不應放置於病人直接治療區域。
- 針對安瓿,先將液體拍至下端、清潔頸部、以紗布或安瓿開啟器朝遠離身體方向折斷,並以濾針或濾鈍器抽取;不得向安瓿注入空氣,若抽入氣泡,應在注射器內處理,不得再排回安瓿。
- 由安瓿抽出的藥液應即時使用;超過即時配製時窗後,未用安瓿藥液依政策丟棄。
- 給藥前,將濾針更換為適用於給藥的針頭/裝置。
- 若安瓿斷口不規則或藥液區有玻璃碎屑,應丟棄該安瓿內容物、安全清理玻璃後,以新安瓿重新開始。
- 計算與抽藥前,先確認醫囑劑量與小瓶說明中的目標最終濃度。
- 從小瓶/仿單/eMAR 來源核實復溶說明(稀釋液類型與體積、最終濃度、儲存條件與使用期限),不得對缺漏資訊自行假設。
- 粉劑藥物復溶時,應使用廠商/藥局指定的精確稀釋液與體積。
- 依指示混合(有需要時採輕滾/旋轉,不搖晃)、確認完全溶解、核實最終濃度,並確認超過可用/保存指引。
- 復溶後若需劑量換算,應以標示之復溶後濃度(mg/mL)作為換算基礎,不可僅以每瓶乾粉量計算。
- 對雙腔小瓶系統,依產品設計啟動內建稀釋液釋放,輕柔旋轉混勻(不可搖晃),抽取前確認無殘留顆粒。
- 若需同針筒混藥,先確認相容性(電子資料庫、機構相容性表或藥師諮詢),並使總體積維持於途徑/部位限制內(例如 ID ⇐ 0.5 mL、SQ 通常 ⇐ 1.5 mL,IM 上限依部位/年齡調整)。
- 當同時混合小瓶與安瓿藥物時,先抽取小瓶藥物,再執行安瓿濾針流程,最後更換為途徑適用給藥針頭。
- 胰島素混合遵循醫囑胰島素特異順序(clear before cloudy):常見做法為先向混濁 NPH 注入空氣但不抽藥,再向 regular 注入空氣並先抽 regular,之後回到 NPH 抽取至醫囑總量;選擇可精確量測混合總劑量的胰島素注射器,且不得混合不相容胰島素類型(例如 glargine/detemir 與其他胰島素)。
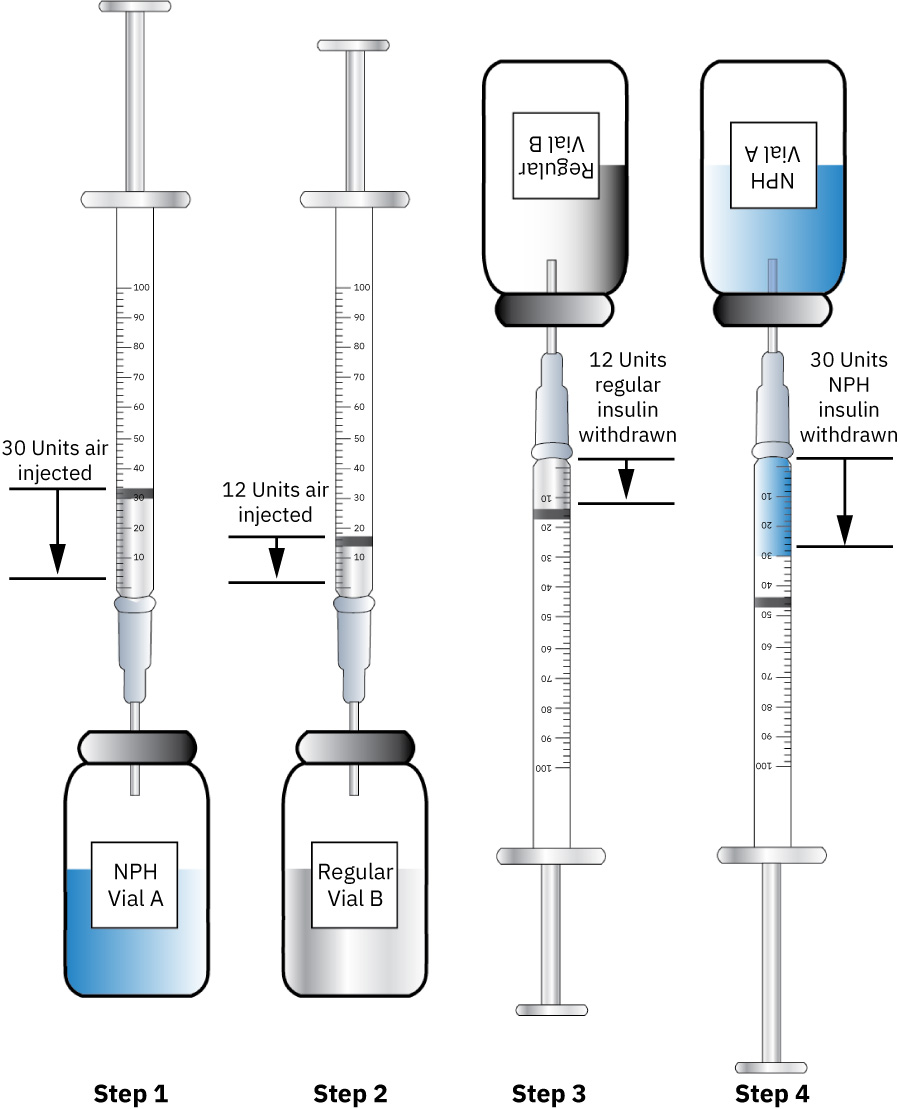 Illustration reference: OpenStax Clinical Nursing Skills Ch.12.
Illustration reference: OpenStax Clinical Nursing Skills Ch.12. - 針對預充注射器/卡匣,核對卡匣完整性、效期與體積是否符合醫囑劑量;接上所需推桿/針頭組件,並依產品說明處理空氣(包含規定需保留氣泡時,如 enoxaparin 產品)。
- 對可重複使用之單劑量卡匣固定器,每次使用間需消毒固定器表面;若以針頭/注射器自卡匣抽藥,不可向卡匣系統注入空氣。
- 對自動注射裝置,確認途徑/部位適配性,並依產品特異啟動順序安全給入預載單劑量。
- 危害性/細胞毒性藥物復溶時,應使用規定防護控制與 PPE,並依政策交由受訓藥局專業人員調配。
- 一次只配製一支藥物注射器/裝置;不可預先為空注射器貼標。
- 除非在床邊立即給藥,否則配製完成藥物需依政策貼標;若配製者與給藥者不同,標示需包含稀釋液類型/體積、稀釋液效期與藥物可用截止時間。
- 檢查最終配製品顏色/澄清度/完整性變化,受損產品不可給藥。
- 在配製流程中依政策完成用藥權核對節點(例如選藥、配製與給藥前核對)。
- 銳器應立即丟棄(包含已開安瓿玻璃置入銳器盒),且不可重複使用注射器/針頭組件。
- 紀錄配製細節、劑量、給藥途徑與反應計畫。
常見錯誤
- 重複使用單劑量小瓶 → 污染與感染風險。
- 安瓿抽取未使用濾針 → 顆粒污染風險。
- 稀釋液錯誤或復溶體積錯誤 → 不安全濃度與劑量錯誤。
- 混合不相容藥物或混合體積過大 → 沉澱/微粒形成、效價改變、毒性或吸收不良風險。
- 以細小/高針規針頭抽取高黏稠藥液 → 彎針/斷針與針扎風險。
- 針頭尺寸與途徑/體型/體積不匹配 → 疼痛、瘀青、給藥不完整或局部組織受損風險。
- 漏標多劑量小瓶開封日期/BUD,或將小瓶防塵蓋視為無菌 → 可預防污染風險。
- 污染注射器活塞桿或 Luer 連接表面 → 注射器內容污染與感染風險。
- 使用來自破損/碎屑污染安瓿的藥液 → 栓塞、靜脈炎、肉芽腫或發炎性損傷風險。
- 向安瓿注入空氣或將已抽入氣泡排回安瓿 → 劑量污染與玻璃微粒暴露風險。
- 移除預充注射器規定應保留的氣泡(例如 enoxaparin 產品) → 劑量輸注不完整風險。
- 向非設計可注氣的卡匣系統注入空氣 → 膠塞噴出與藥液流失/受傷風險。
- 在未依規定防護/PPE 流程下復溶危害性藥物 → 職業暴露風險。
- 混藥時超過途徑/部位體積上限 → 疼痛、滲漏與吸收不可靠風險。
- 胰島素順序錯誤或混合不相容長效胰島素劑型 → 血糖反應不穩風險。
- 預先為空注射器貼標或讓已配製注射器無人看管 → 錯藥/錯病人風險。
- 以乾粉量、稀釋液體積或估算最終體積置換取代標示復溶後濃度 → 劑量計算錯誤風險。
相關
- 皮內給藥 - 配製後 ID 特異上限與技術限制。
- 皮下注射給藥 - SQ 途徑體積/角度要求。
- 肌內給藥 - 已配製劑量的 IM 部位與體積決策。
- 靜脈給藥安全 - IV 相容性與監測要求。
- 銳器處置與針扎傷應對 - 配製與給藥期間必須落實的銳器安全。