阿茲海默症
要點
- 阿茲海默症是最常見的 失智症 亞型,會造成記憶、語言、判斷與日常功能進行性下降。
- AD 是一種伴隨皮質萎縮與進行性神經元流失的神經退化性疾病。
- 儘管多數病例發生於 65 歲後,40-50 歲也可能出現早發型表現。
- 目前 AD 藥物治療無法治癒,通常僅能在症狀層面有限減緩下降。
- 盛行率隨年齡顯著上升(約 5% 為 65-74 歲、13.2% 為 75-84 歲、33.4% 為 85 歲以上)。
- 家庭照護者常提供高強度無償支持,且有較高身心負擔風險。
- 以抗發炎與抗氧化為重點的飲食型態(例如地中海式飲食)可作為輔助照護,支持較慢認知下降。
病理生理
阿茲海默症(AD)是進行性神經退化性疾病,也是高齡者顯著認知下降的主要原因之一。與預期老化變化相比,AD 涉及更快速的大腦結構與功能惡化。
早期描述變化包含進行性皮質萎縮與神經元退化,並隨時間出現認知與獨立性受損加重。
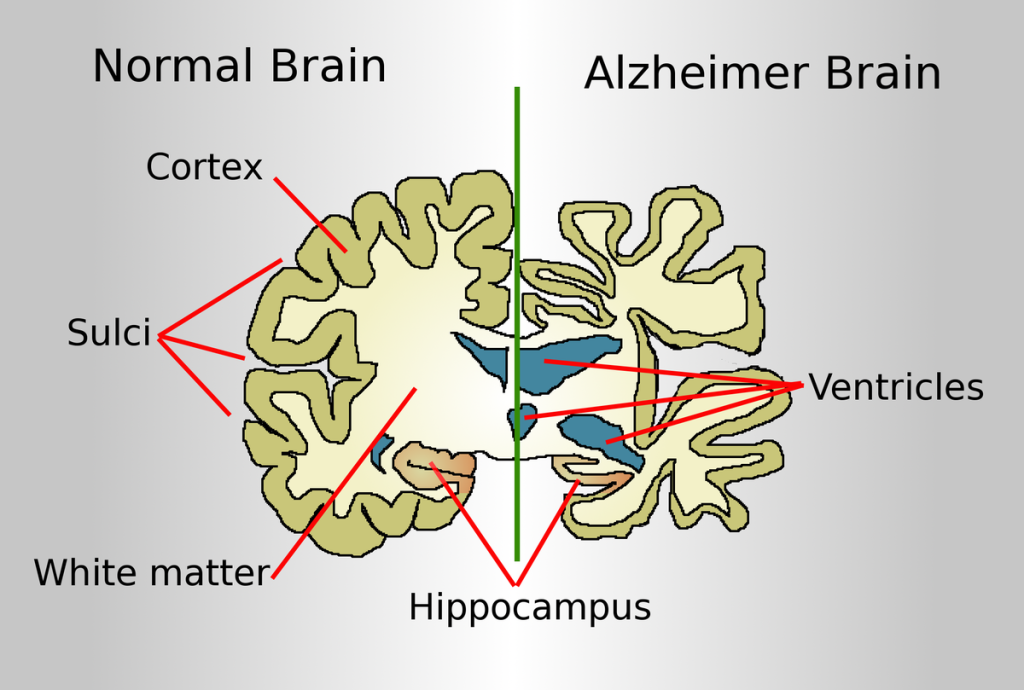 Illustration reference: OpenRN Health Alterations Ch.9.5.
Illustration reference: OpenRN Health Alterations Ch.9.5.
標誌性顯微病理發現包含神經纖維纏結與神經炎斑塊。異常 beta-amyloid 與 tau 蛋白沉積會破壞神經元間訊號傳遞並加速神經退化。
初始損傷常累及記憶、語言與思考相關區域,因此早期表現常見短期記憶喪失與語言/執行功能下降。病理性腦部改變可能在明確臨床症狀前多年即已開始。
神經傳導物質失衡(包含乙醯膽鹼、正腎上腺素、多巴胺與血清素下降)也與認知惡化及新記憶保留困難相關。
分類
- 疾病背景:65 歲以上成人最常見的 失智症 亞型。
- 功能影響:記憶、語言、理解、注意、推理與判斷能力進行性缺損。
- 核心病理:神經纖維纏結與神經炎斑塊造成神經元溝通受損。
- 不可改變風險因子:年齡增長、高齡女性、一等親家族史,以及部分遺傳/發展易感情境。
- 可改變與情境性風險因子:菸草暴露、不活動、心代謝控制不良、認知/社交刺激不足,以及部分藥物/毒素相關因素。
- 臨床分期:
- 臨床前 AD:存在生物標記/腦部改變,但無明確臨床症狀。
- AD 所致 MCI:輕度症狀,可能尚未干擾日常功能。
- AD 所致輕度失智:早期症狀群並逐步影響 IADL(常先影響財務與複雜規劃),對財務剝削/詐騙的脆弱性增加。
- AD 所致中度失智:混亂加劇、多步驟 ADL 困難、遊走/失禁、幻覺-妄想及日落症候群等行為症狀。
- AD 所致重度失智:溝通與活動能力顯著下降,伴吞嚥困難、厭食/體重下降及完全 ADL 依賴,併發症風險高(例如 吸入性肺炎、血栓、感染/敗血症)。
- 照護背景:對 ADL 與居家安全支持需求高。
護理評估
NCLEX 重點
從照護開始即同時評估病人認知下降與照護者健康影響。
- 評估基線認知與功能狀態,並隨時間追蹤進展。
- 評估起病時間、持續時間與進展型態,並區分慢性下降與急性 譫妄 疊加。
- 評估早期預警型態改變(記憶影響日常生活、規劃/解題能力下降、熟悉任務困難、時空混亂、視空間困難、找詞變化、反覆放錯物品且無法回溯、不良判斷、社交退縮及情緒-人格變化)。
- 評估 照護者負擔、疲勞、因應壓力與維持居家支持能力。
- 評估與判斷受損及自我管理下降相關的安全風險。
- 當病人病識感受限時,使用家屬或重要他人補充病史。
- 使用與識字程度與能力匹配的認知工具(例如 MMSE、Mini-Cog、set test、畫鐘篩檢)追蹤下降趨勢。
- 整合診斷背景:AD 仍以組織病理為最終確證,臨床檢查可包含 CSF beta-amyloid/tau 與 PET 影像支持。
- 使用診斷型態排除類似疾病:血液檢驗尋找可逆因子(例如維生素或 甲狀腺疾病)、MRI 評估區域萎縮/排除其他病因、PET 評估低代謝,CT 主要用於結構性鑑別診斷。
- 在鑑別評估中檢查可逆性認知受損因素(例如維生素 B12、甲狀腺與肝臟相關病因)。
- 篩檢憂鬱及其他情緒障礙,因其可能與記憶和專注力抱怨重疊。
護理介入
- 採用結構化認知與功能再評估,以指引分期適配支持計畫。
- 強化「食物優先」神經保護型態(水果/蔬菜、全穀、魚類、堅果、以橄欖油為主脂肪),並限制超加工高碳水攝取,以減輕代謝-發炎負擔。
- 及早整合照護者支持策略,包含轉介喘息服務與社區支持服務。
- 隨認知下降進展,強化居家安全規劃。
- 使用轉移注意/分散策略、低刺激環境與一致作息以減少躁動。
- 在重度階段痛苦情境中優先採肯認式回應;避免對抗性現實導向,以免加劇躁動。
- 建立傷害預防計畫:空間整潔、照明充足、遊走預防/身分識別支持及分期適配監督。
- 規劃如廁/失禁照護、營養支持(手拿食物、必要時調整質地/液體)、促進睡眠的白天活動及簡化溝通提示。
- 在急性照護情境中,最大化觀察、減少病房轉換、監測遊走風險,並在約束路徑前優先使用非藥物鎮靜策略。
- 使用結構化疼痛評估(包含適用於晚期 失智症 溝通受限的工具),並及早處理不適以降低躁動升級。
- 確診後及早協調個案管理轉介,用於長期支持服務規劃與照護者支持。
- 強化照護者減壓規劃:務實期待、每日喘息休息、自我照護常規、支持團體/專線使用,以及及早預立照護/法律規劃。
- 針對 AD 藥物教導:不可突然停藥、漏服後不可加倍、ER 膠囊劑型不可壓碎/咀嚼。
照護者健康風險
長期無償照護可能造成身心狀態下降,進而降低照護品質與安全性。
藥理學
藥物管理依分期與症狀而定,應與非藥物安全、溝通及照護者支持介入整合。現有藥物無法逆轉 AD,通常僅提供有限時間的症狀性效益。
| 藥物類別 | 範例 | 主要護理注意事項 |
|---|---|---|
| 類澱粉蛋白標靶藥物 | lecanemab(aducanumab 已於 2024 年由製造商停產) | 用於部分輕度階段路徑的靜脈治療;監測 MRI 相關類澱粉蛋白影像異常及輸注/過敏反應(例如發燒、心悸、呼吸困難、血管性水腫)。 |
| 膽鹼酯酶抑制劑 | donepezil、rivastigmine、galantamine | 存在腸胃道反應與心搏過緩風險;監測心率、頭暈與耐受性。 |
| 麩胺酸調節藥物 | memantine | 用於中重度 AD;監測頭暈/混亂/[constipation]、腎功能及與尿液 pH 相關交互作用風險(例如 sodium bicarbonate、碳酸酐酶抑制劑與 thiazides)。 |
| 認知聯合製劑 | donepezil + memantine ER(Namzaric) | 當 donepezil 已建立治療方案時用於中重度 AD;在每週 memantine 滴定期間監測精神狀態與 ADL 軌跡。 |
| 食慾素受體拮抗劑 | suvorexant | 監測隔日警覺性、情緒/自殺風險關注與呼吸狀態。 |
| 用於重度攻擊行為/精神病性症狀的精神藥物 | risperidone、olanzapine、carbamazepine、valproic acid | 屬化學性約束情境;遵循政策層級防護並頻繁再評估必要性。 |
臨床判斷應用
臨床情境
一名高齡者出現進行性短期記憶下降,與配偶同住於家中;配偶表示因日常監督需求增加而極度疲憊。
- 辨識線索:進行性認知下降並伴照護者壓力。
- 分析線索:AD 進展正同時影響病人安全與照護者健康。
- 確立優先假設:即刻優先項為安全穩定與照護者支持。
- 提出解決方案:依分期支持更新照護計畫並連結社區支持資源。
- 採取行動:實施安全常規並啟動照護者支持轉介。
- 評估結果:在持續監測功能同時,居家安全與照護者因應能力改善。
評值應持續進行:再評估認知/功能趨勢、檢視新診斷資料,並在結果部分達成或未達成時修訂照護計畫。
相關概念
- 失智症 - 更廣泛重度神經認知障礙架構與鑑別背景。
- 乙醯膽鹼酯酶抑制劑 - 以 donepezil 為核心的膽鹼性藥物治療與給藥安全。
- 照護失智症個案 - 日常溝通與行為支持策略。
- 照護者角色壓力 - 長期家庭照護中的心理社會與功能負擔。
- 神經系統 - 疾病理解所需神經解剖與神經傳導基礎。
自我檢查
- 為什麼在阿茲海默症照護規劃中必須及早開始照護者評估?
- 哪些發現最能提示由輕度功能影響進展至更高風險依賴?
- 隨認知下降惡化,護理優先項應如何調整?