阿尔茨海默病
要点
- 阿尔茨海默病是最常见的 失智症 亚型,可导致记忆、语言、判断与日常功能进行性下降。
- AD 是一种伴皮质萎缩和进行性神经元丢失的神经退行性疾病。
- 尽管多数病例发生在 65 岁后,40-50 岁也可出现早发型表现。
- 当前 AD 药物治疗无法治愈,通常仅能在症状层面有限减缓下降。
- 患病率随年龄显著上升(约 5% 为 65-74 岁,13.2% 为 75-84 岁,33.4% 为 85 岁以上)。
- 家庭照护者常提供高强度无偿支持,并处于较高身体与情绪负担风险中。
- 以抗炎与抗氧化为重点的饮食模式(例如地中海式饮食)可作为辅助照护支持更慢的认知下降。
病理生理
阿尔茨海默病(AD)是进行性神经退行性疾病,也是老年人显著认知下降的主要原因之一。与预期衰老变化相比,AD 涉及更快的脑结构与功能恶化。
早期已描述的变化包括进行性皮质萎缩和神经元退变,并随时间出现认知与独立性受损加重。
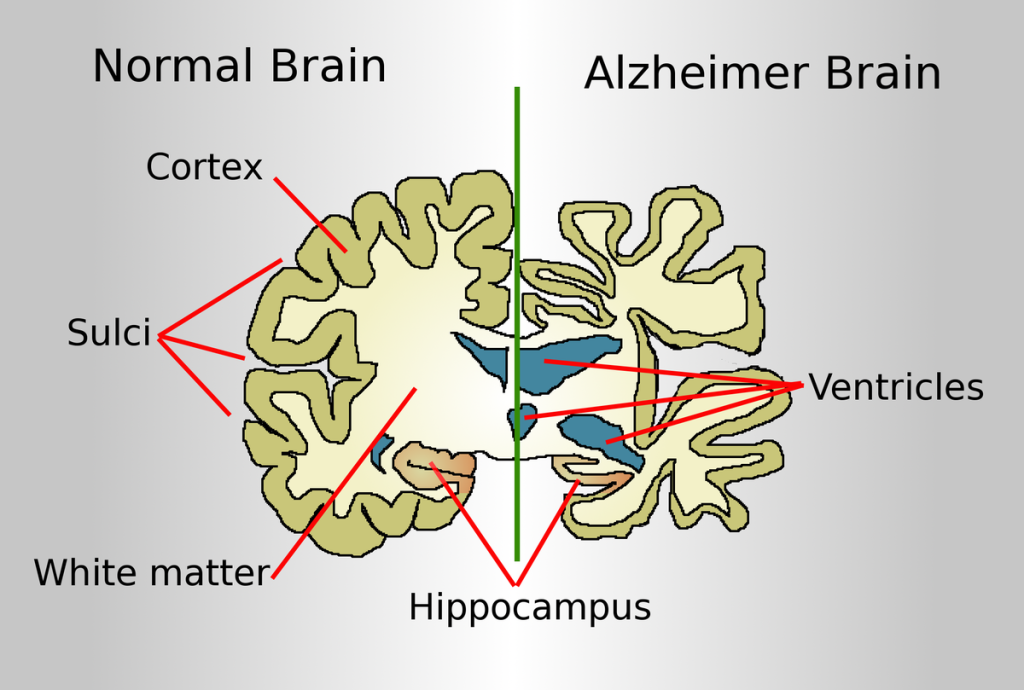 Illustration reference: OpenRN Health Alterations Ch.9.5.
Illustration reference: OpenRN Health Alterations Ch.9.5.
标志性显微病理发现包括神经原纤维缠结和神经炎斑块。异常 β-淀粉样蛋白与 tau 蛋白沉积会破坏神经元间信号传递并加速神经退行。
初始损伤常累及记忆、语言与思维相关区域,因此早期表现常包括短期记忆丧失以及语言/执行功能下降。病理性脑改变可在明确临床症状出现前多年即已开始。
神经递质失衡(包括乙酰胆碱、去甲肾上腺素、多巴胺和血清素降低)也与认知恶化和新记忆保持困难相关。
分类
- 疾病背景:65 岁以上成人最常见的 失智症 亚型。
- 功能影响:记忆、语言、理解、注意、推理与判断能力进行性缺损。
- 核心病理:神经原纤维缠结与神经炎斑块导致神经元通信受损。
- 不可改变风险因素:年龄增长、老年组女性、家族史/一级亲属,以及部分遗传/发育易感背景。
- 可改变与情境性风险因素:烟草暴露、活动不足、心代谢控制不良、认知/社交刺激不足,以及部分药物/毒素相关因素。
- 临床分期:
- 临床前 AD:存在生物标志物/脑改变,但无明确临床症状。
- AD 所致 MCI:轻度症状,可能尚未干扰日常功能。
- AD 所致轻度失智:早期症状群并逐步影响 IADL(常先影响财务与复杂计划),对财务剥削/诈骗的易感性升高。
- AD 所致中度失智:混乱加重、多步骤 ADL 困难、游走/失禁、幻觉-妄想及日落综合征等行为症状。
- AD 所致重度失智:沟通与活动能力显著下降,伴吞咽困难、厌食/体重下降及完全 ADL 依赖,并发症风险高(例如 吸入性肺炎、血栓、感染/脓毒症)。
- 照护背景:对 ADL 与居家安全支持的照护需求高。
护理评估
NCLEX 重点
从照护开始即同时评估患者认知下降和照护者健康影响。
- 评估基线认知与功能状态,并随时间追踪进展。
- 评估起病时间、持续时间与进展模式,并区分慢性下降与急性 谵妄 叠加。
- 评估早期预警模式变化(记忆影响日常生活、计划/解决问题能力下降、熟悉任务困难、时空混乱、视空间困难、找词变化、反复放错物品且无法回溯、判断变差、社交退缩及情绪-人格变化)。
- 评估 照护者负担、疲劳、应对压力及维持居家支持的能力。
- 评估与判断受损及自我管理下降相关的安全风险。
- 当患者病识感受限时,使用家属或重要他人提供补充病史。
- 使用与识字水平和能力匹配的认知工具(例如 MMSE、Mini-Cog、set test、画钟筛查)追踪下降趋势。
- 整合诊断背景:AD 仍以组织病理为最终确证,临床检查可包括 CSF β-淀粉样蛋白/tau 和 PET 影像支持。
- 使用诊断模式排除拟似疾病:通过血液检测寻找可逆因素(例如维生素或 甲状腺疾病)、磁共振成像(MRI)评估区域萎缩/排除其他病因、PET 评估低代谢,计算机断层扫描(CT)主要用于结构性鉴别诊断。
- 在鉴别评估中检查可逆性认知受损因素(例如维生素 B12、甲状腺及肝相关病因)。
- 筛查抑郁及其他情绪障碍,因为其可与记忆和注意力抱怨重叠。
护理干预
- 采用结构化认知与功能复评,以指导分期适配的支持计划。
- 强化“食物优先”的神经保护模式(水果/蔬菜、全谷物、鱼类、坚果、以橄榄油为主的脂肪),并限制超加工高碳水摄入,以减少代谢-炎症负担。
- 早期整合照护者支持策略,包括转介喘息服务与社区支持服务。
- 随认知下降进展强化居家安全规划。
- 使用转移注意/分散策略、低刺激环境与一致作息以减少激越。
- 在重度阶段痛苦情境中优先采用确认式沟通;避免对抗性现实定向,以免加剧激越。
- 制定损伤预防计划:空间整洁、照明充足、游走预防/身份识别支持及分期适配监督。
- 规划如厕/失禁照护、营养支持(手拿食物、按需调整质地/液体)、促进睡眠的白天活动及简化沟通提示。
- 在急性照护环境中,最大化观察、尽量减少病房转移、监测游走风险,并在约束路径前优先使用非药物镇静策略。
- 使用结构化疼痛评估(包括适用于晚期 失智症 沟通受限的工具),并早期处理不适以降低激越升级。
- 在确诊后尽早协调个案管理转介,用于长期支持服务规划与照护者支持。
- 强化照护者减压规划:现实预期、每日喘息休息、自我照护常规、支持小组/热线使用,以及早期预立照护/法律规划。
- 对 AD 药物教育:不可突然停药,漏服后不可加倍,ER 胶囊制剂不可压碎/咀嚼。
照护者健康风险
长期无偿照护可导致身体与情绪状态下降,进而降低照护质量与安全性。
药理学
药物管理依分期与症状而定,应与非药物安全、沟通及照护者支持干预整合。现有药物不能逆转 AD,通常仅提供有限时长的症状性获益。
| 药物类别 | 示例 | 关键护理注意事项 |
|---|---|---|
| 靶向淀粉样蛋白药物 | lecanemab(aducanumab 已于 2024 年由制造商停产) | 用于部分轻度阶段路径的静脉治疗;监测磁共振成像(MRI)相关淀粉样蛋白影像异常及输注/过敏反应(例如发热、心悸、呼吸困难、血管性水肿)。 |
| 胆碱酯酶抑制剂 | donepezil、rivastigmine、galantamine | 存在胃肠道反应与心动过缓风险;监测心率、头晕与耐受性。 |
| 谷氨酸调节药物 | memantine | 用于中重度 AD;监测头晕/意识混乱/[constipation]、肾功能及与尿液 pH 相关的相互作用风险(例如碳酸氢钠、碳酸酐酶抑制剂和噻嗪类)。 |
| 认知联合制剂 | donepezil + memantine ER(Namzaric) | 当 donepezil 已建立方案时用于中重度 AD;在每周 memantine 滴定期间监测精神状态与 ADL 轨迹。 |
| 食欲素受体拮抗剂 | suvorexant | 监测次日警觉性、情绪/自杀风险关注及呼吸状态。 |
| 用于严重攻击行为/精神病性症状的精神药物 | risperidone、olanzapine、carbamazepine、丙戊酸 | 属于化学约束情境;遵循政策级防护并频繁复评必要性。 |
临床判断应用
临床情景
一名老年人出现进行性短期记忆下降,居家与配偶同住;配偶报告因日常监督需求增加而极度疲惫。
- 识别线索:进行性认知下降并伴照护者压力。
- 分析线索:AD 进展正在同时影响患者安全与照护者健康。
- 确定优先假设:即刻优先项为安全稳定与照护者支持。
- 提出解决方案:按分期支持更新照护计划并连接社区支持资源。
- 采取行动:实施安全常规并启动照护者支持转介。
- 评估结局:在持续监测功能的同时,居家安全与照护者应对能力改善。
评价应持续进行:复评认知/功能趋势,审阅新诊断数据,并在结局部分达成或未达成时修订照护计划。
相关概念
- 失智症 - 更广泛的重度神经认知障碍框架与鉴别背景。
- 乙酰胆碱酯酶抑制剂 - 以 donepezil 为中心的胆碱能药物治疗与给药安全。
- 照护失智症来访者 - 日常沟通与行为支持策略。
- 照护者角色紧张 - 长期家庭照护中的心理社会与功能负担。
- 神经系统 - 疾病理解所需神经解剖与神经传递基础。
自我检查
- 为什么在阿尔茨海默病照护规划中必须尽早开始照护者评估?
- 哪些发现最能提示从轻度功能影响进展到更高风险依赖?
- 随认知下降加重,护理优先项应如何调整?